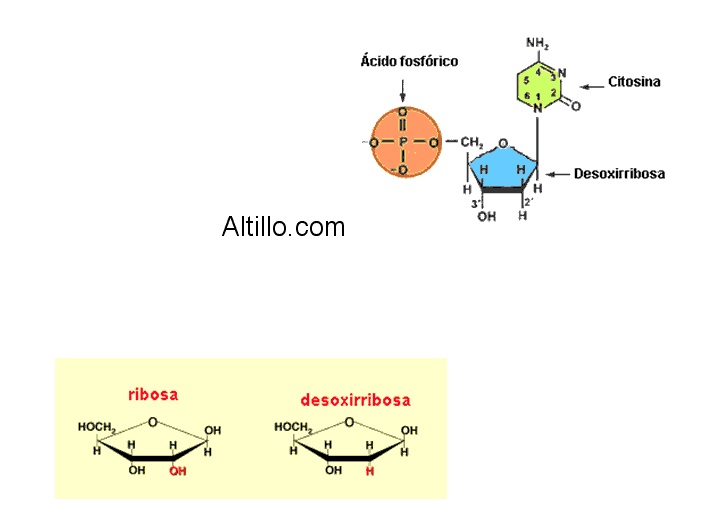
1.2.- Características de los seres vivos. 1) Tienen homogeneidad en su composición química: TODOS están constituidos por carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre. Estos se los encuentra en las moléculas orgánicas, como hidratos de carbono, lípidos, proteínas y ácidos nucleicos. Entre estas, se destaca el ADN, que dirige, controla y regula las reacciones químicas que permiten el desarrollo de la vida. 2) Están formados por células: son las unidades estructurales y funcionales de los seres vivos. Generalmente son microscópicas, y desarrollan todas las funciones
necesarias que mantienen la vida. Los seres vivos pueden ser unicelulares, ó pluricelulares. 3) Son estructuras complejas y altamente organizadas: esto le permite cumplir con las funciones vitales, y aprovechar al máx. la materia y energía que intercambian con el entorno. 4) Tienen metabolismo: realizan todas las reacciones químicas que ocurren en el interior de sus células. Estas reacciones son específicas y ordenadas, de acuerdo con la demanda de la célula. Se mantienen a través del intercambio constante de materia y energía con el entorno. Por ejemplo, pueden elaborar moléculas y estructuras indispensables para la vida, ó bien, eliminar aquellas que no se utilizan. 5) Mantienen su homeostasis: mantienen constantes (en equilibrio) las condiciones físicas y químicas de su medio interno, por medio de un sistema de control y regulación. Por ejemplo, se crea un estado de equilibrio en la concentración de oxígeno y dióxido de carbono, en el pH, en la concentración de nutrientes y productos de desecho, la concentración de sales, el volumen y presión de fluidos extracelulares, la T°, etc 6) Tienen crecimiento: aumentan de tamaño, y algunos también se desarrollan. Los organismos pluricelulares crecen por aumento de la cantidad de células que los componen. En tanto que, los organismos unicelulares crecen por el aumento de tamaño de su célula hasta un cierto punto, y cuando éste se detiene, se forman dos organismos iguales. 7) Poseen irritabilidad: son las reacciones/respuestas que tienen frente a los estímulos del medio externo. Los animales por ejemplo, pueden ubicar su alimento, su pareja, o una fuente de peligro. La respuesta de sus estímulos entonces, dependerá de la especie de la que se trate. En los vegetales en cambio, existen sólo 3 movimientos (tropismos) como respuesta a los estímulos. El fototropismo es el movimiento de las plantas, frente al estimulo luminoso. El geotropismo es el estímulo producido por la gravedad, que genera distintas respuestas en tallos y raíces. Y el fototaxismo, es una respuesta o reacción a la luz. Si es positivo, el vegetal se dirige a la luz; si es negativo, escapa de ella. 8) Tienen reproducción: generan descendientes que los podrían reemplazar biológicamente. Esta puede ser asexual o sexual. En la primera, un individuo genera otro idéntico a sí mismo, por divisiones mitóticas que producen células idénticas en cantidad, y tipo de ADN con respecto a la célula original. En la segunda, intervienen células especializadas que poseen un núcleo con la mitad de la información genética que la célula original. En esta, la célula primero se divide por meiosis (división celular reduccional), y luego ocurre la fusión de una célula femenina con una masculina (fecundación). Finalmente, el individuo resultante poseerá características de ambos progenitores. 9) Pueden modificar el ambiente en el que viven: como sistemas abiertos, intercambian materia y energía con el entorno, lo que cambia el medio en el que viven, transformándolo de manera perceptible o no, rápida o lentamente. Por ejemplo, el pH del suelo cambia según la vegetación que sostenga. El pH de la tierra de los pinos, será más ácido que el del suelo de una selva con diversidad de especies. 10) Pueden evolucionar: referido a la condición de cambiar. Los seres vivos pueden modificar su estructura y/ó funcionamiento de forma permanente, y transmitirla también a sus descendientes. Esto se asocia con la información genética que se hereda de generación en generación, y se manifiesta como alteraciones en esta información ó “mutaciones”, que generan variabilidad dentro de una especie. Los cambios son producidos de manera arbitraria (al azar - involuntarios), y es por ello que pueden ser ventajosos (favoreciendo su adaptación al medio, su competitividad, y su reproducción), desventajosos (perjudicándolos hasta incluso la extinción), o neutros si no alteran la estructura o funcionamiento del ser vivo. 1.3.- Agrupación de los seres vivos en 5 reinos. El sistema de clasificación actual, deriva de la conocida “clasificación zoológica” (o clasificación de pirámide invertida), creada por el naturalisa sueco von Linnaeo, y es el que REEMPLAZA al antiguo (pero más novedosos que la pirámide) sistema propuesto por Chatton. El mismo, cuenta con la “moderna” separación de los seres vivos en 5 reinos y 3 dominios, según sus características. DOMINIO ARCHAEA BACTERIA EUKARAYA REINO Monera Protista Fungi Vegetal Animal TIPO DE CELULA Procariota Eucariota Eucariota Eucariota Eucariota CANTIDAD DE CÉLULAS UNIcelular UNI y PLURIcelular PLURIcelular PLURIcelular PLURIcelular TIPO DE NUTRICION Ambas Ambas Heterótrofa Autótrofa Heterótrofa NIVEL DE ORGANIZACÓN Celular Celular y multicelular Celular y tisular Sistema de Órganos De Tisular hasta Sistema de Órganos EJEMPLOS Escherichia coli, Cianoficeas Cianobac-terias, protozoos. Algas rojas, protozoos Mohos, hongos Plantas vasculares Medusa, tenia, lobo, hombre. CAPÍTULO 2: Organización general de la célula. 2.1.- Organización general de las células. Todos los seres vivos están compuestos por células y productos celulares. Éstas, se clasifican en 2 tipos: • Célula procariota o procarionte: las más sencillas, no poseen núcleo, su ADN está disperso por el citoplasma, y sus organelas están diferenciadas. • Célula eucariota o eucarionte: tienen un núcleo diferenciado donde esta contenido su ADN, y un complejo sistema de endomembranas. A su vez, desarrolla funciones específicas en los organismos pluricelulares, de manera armónica, coordinada, y eficiente. Sus principales funciones dentro de un organismo son: • Reproducción (transmisión de la información hereditaria = ADN). • Producción y control de la estructura y de sus funciones. • Síntesis de biomoléculas. • Provisión de energía (ATP, GTP, metabolización de O2 / respiración). • Digestión, para la utilización de materiales y eliminación de desechos (absorción, asimilación, excreción). • Separación y comunicación (irritabilidad, motilidad, contractilidad, permeabilidad). 2.2.- La Teoría celular: aspectos genéticos y bioquímicos básicos. La teoría celular, postula que la célula: • Es la unidad más pequeña de vida. • Se la considera unidad estructural y funcional de los seres vivos: o Estructural porque no pueden dividirse en partes, ya que se mueren. o Funcional, porque cumplen con todas las funciones vitales de la materia viva (respirar, alimentarse, reproducirse, etc.). • Las propiedades de un organismo, dependen de las propiedades cada una de sus células individuales. • Proviene SOLO de otras células ya preexistentes. La herencia de la información genética, mantiene la continuidad y se la transmite a la descendencia. 2.3.- Aspectos genéticos y bioquímicos básicos de la célula. Las células están formadas químicamente por agua, y moléculas orgánicas: unidad de composición (ácidos nucleicos, proteínas, glúcidos, lípidos). También contienen (en menor proporción), iones, ADN y ARN. A continuación, podemos ver algunos de sus aspectos físicos y genéticos. Tipo de célula. PROCARIOTA EUCARIOTA Nivel de organización. Desde el celular hasta el colonial. Desde el celular, al sist. De órganos. Tamaño. Entre 0,1 y 5 μm de longitud. Entre 10 a 100 μm de longitud. Movilidad intracelular Ausente. Presente. Movimiento de organelas y división celular. Genoma (ADN) Un solo cromosoma circular presente en el protoplasma. ADN NO asociado a proteínas histonas. Varios cromosomas NO circulares, con ADN asociado a proteínas histonas, ubicado en el núcleo celular. Biosíntesis proteica (ARN) Ocurre en el protoplasma (entre el citoplasma y el núcleo). El ARNm se transcribe y traduce, sin maduración. Transcripción, ensamblaje de ribosomas y maduración del ARNm en el núcleo. Posterior traducción en el citoplasma. División celular Fisión binaria transversal. 2 tipos: Mitosis o división en la reproducción asexual; y meiosis o división en la reproducción sexual. Pared celular. Presente en algunos grupos, compuesta por peptidoglucanos. Presente en vegetales y hongos (reino Fungi) Cilios y flagelos. Cilios ausentes, y flagelos simples con un solo filamento. Presentes en protistas, animales y plantas criptógamas. Metabolismo. Anaeróbico y aeróbico. Anaeróbico y aeróbico. Citoesqueleto. Ausente. Presente. Está formado por microtúbulos, microfilamentos filamentos intermedios. 2.4.- Organización general de las células procariotas. 2.4.1.- Características generales. • Son los organismos celulares más pequeños. Su tamaño varía con la especie, pero generalmente miden entre 0,2 y 5 μm (micrómetros). • Tienen una rápida reproducción celular. • Pueden sobrevivir en ambientes muy diversos, tanto en condiciones aeróbicas como anaeróbicas, de forma autótrofa o heterótrofa. • No poseen núcleo definido y su material genético está distribuido por el citoplasma, en un espacio denominado “nucleoide”. • Carecen de membranas internas o envoltura nuclear. • Las más simples conocidas, son las micoplasmas (organelas de la vida parasitaria), y la más estudiada es la bacteria escherichia coli, entre otras. 2.4.2.- Clasificación. Según su forma, se dividen en: • Cocos (forma esférica): si dos células permanecen unidas se forman diplococos. Si éstps a su vez permanecen unidos también, se formarán estreptococos (cadenas de cocos), o estafilococos (racimos). • Bacilos (forma cilíndrica): si dos células permanecen unidas se forman diplobacilos. Si éstos últimos permanecen unidos entre sí, se formarán estreptobacilos (cadenas de bacilos). • Espirilos (forma espiral) • Vibriones (forma de coma). 2.4.3.- Estructura. • Cápsula: es la estructura más superficial. Está formada por la acumulación de material viscoso, ubicado por fuera de la pared celular. Químicamente, tiene polisacáridos o polipéptidos. Puede ser rígida (consistente, con límites definidos), ó bien, flexible (poco consistente deformable y sin límites), o sino integral (asociada a la pared celular). Tiene la capacidad de adherirse a otras células o sustratos inertes. NO ES CONSTANTE, sino que está presente SOLO en BACTERIAS con cierta patogenisidad. • Flagelos: son extensiones largas y delgadas formadas por monómeros de flagelina (proteína globular). Pueden estar en la superficie de la célula o en el poro celular. Sobresale de la célula como un filamento desnudo, que atraviesa la membrana y pared celular, otorgándole a la célula movimiento, y adhesión a fuentes alimenticias. • Pelos/Pili: son varillas cilíndricas rígidas que, en general, están presentes en gran número. Su función es la adhesión a una fuente alimenticia. • Pared celular: rodea a la membrana plasmática. Su función es dar protección osmótica al interior celular. Para ello, regula el paso de sustancias a través de sus poros, permitiendo (de manera restringida) la comunicación con el medio exterior. A su vez, brinda un espacio periplásmico para las enzimas de transporte, hidrolíticas, etc.
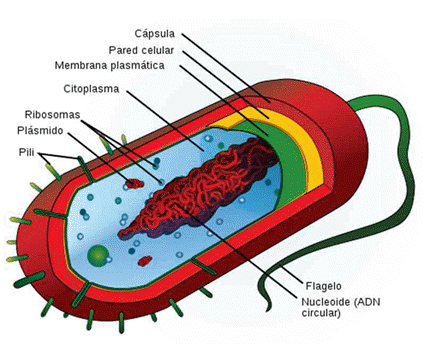
Puede ser rígida o flexible, pero siempre mantiene su forma para evitar la lisis. En algunos seres vivos como los microplasmas, está ausente Está formada por lípidos, proteínas y polisacáridos. Los peptidoglucanos por ej, permiten clasificar a las bacterias como “Gram Positivas”, si su pared celular posee una importante cantidad de éste, o “Gram negativas”, si poseen poca cantidad. • Membrana plasmática: se ubica dentro de la pared celular, rodeando al citoplasma. Es flexible y semipermanente. Está formada por una bicapa lipídica y proteínas asociadas. NO posee colesterol ni otros esteroides. Se encarga de regular el ingreso de sustancias, luego de que atraviesen la pared celular. o Mesosoma: es una prolongación o pliegue de la membrana, que va hacia el interior de la célula. Es único y desnudo, porque NO posee proteínas. Estos, actúan durante el proceso de división celular, ya que contienen los sitios de unión para las moléculas de ADN. También forman un tabique o pared entre las dos células hijas. • ADN: es una sola molécula circular, desnuda, enrollada y cerrada. Está asociada a proteínas no histónicas, llamadas cromosoma. Esta molécula se duplica antes de la división celular, y cada uno de los dos cromosomas hijos, se une a un punto diferente de la membrana celular, que al alargarse, permite la separación de éstos dos. • Plásmidos: pequeña cantidad de material genético, circular y auto-replicante, que contienen ALGUNAS bacterias. La mayoría de las veces, llevan también ciertos genes que le confieren a las bacterias, resistencia a los antibióticos. Los mismos, se dividen en 2 tipos: plásmidos F, de factor sexual, y plásmidos R, de resistencia a las drogas. Su información NO es vital. • Citoplasma: no está dividido en compartimientos. Es casi homogéneo por la ausencia de organelas limitadas por membrana, y presenta numerosos ribosomas. • Ribosomas: son más chicos que los de la célula eucariota. Se encargan de sintetizar proteínas, y suelen agruparse, formando poliribosomas o polisomas. • Laminillas: son unos pliegues en forma de láminas, asociados a la membrana plasmática, que tienen pigmentos fotosintéticos para alimentarse de forma autótrofa. • Estructuras respiratorias: pliegues muy pequeños en la membrana plasmática que tienen moléculas para realizar respiración aeróbica. 2.5.- Organización general de las células eucariotas.
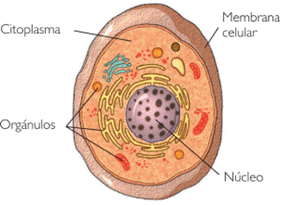
A diferencia de las procariotas, las células eucariotas tienen un sistema de endomembranas que “separan las funciones” en compartimientos diferenciados (organelas/organulos). Estos se encuentran en el citoplasma, lugar donde ocurre la mayoría de las reacciones metabólicas. El nombre “eucariota”, se debe a la presencia de un núcleo. Las mismas, poseen una membrana celular que las envuelve y les permite el intercambio químico con el exterior. Asimismo, una eucarionte puede medir entre 10 y 100 μm, aunque algunos protistas pueden alcanzar los 150 μm. La misma, se puede subdividir en dos tipos: célula animal, y célula vegetal. 2.5.1.- Compartimentalización.
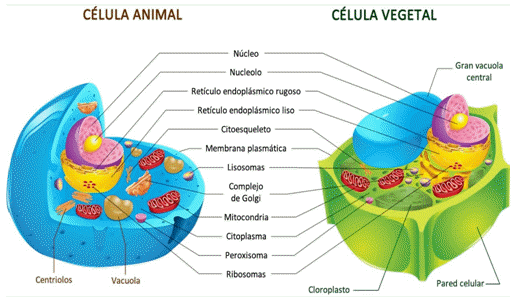
El interior de las eucariontes está dividido en un sistema de compartimientos, rodeados por una membrana. Estos, difieren tanto en su estructura como en la función que cumplen, sin embargo, son pocas las organelas que están presentes en un tipo de célula eucariota, y en otra no. En caso de que sea así, será indicado en la descripción. • Núcleo: ocupa la región central de la célula. Presenta forma esferoidal, y está delimitado por una envoltura de doble membrana con poros. Éste, contiene el material genético. • Vesículas: estructuras delimitadas por membrana, que se encargan de aislar materiales de las diferentes regiones de la célula. • Cisternas: cavidades aplanadas que se extienden a través del citoplasma, subdividiéndolo en compartimientos intercomunicados, de variada forma y tamaño. • Citoesqueleto: red tridimensional de proteínas que da forma a la célula, la sostiene, y posibilita el movimiento interno celular. • Pared celular: SOLO en las células vegetales. Está compuesta de celulosa, y tiene pequeños poros llamados plasmodesmos. Se encarga de proteger a la célula frente a algún desorden estructural. • Compartimentos delimitados por doble membrana: son aquellas organelas donde ocurren reacciones de transformación y almacenamiento de energía útil para la célula. § Cloroplastos: SÓLO están presentes en las células vegetales y autótrofas. Realizan el proceso fotosintético. § Plástidos: SÓLO en células vegetales. Se encargan de almacenar sustancias en reservas. § Mitocondrias: se encuentran libres en el citoplasma, intervienen en la oxidación de moléculas orgánicas (respiración celular aeróbica) y la producción de energía en la célula. • Sistema de endomenbranas. Son aquellos compartimientos celulares que están formados por cisternas, y delimitados por una sola membrana más delgada que la plasmática. o Envoltura nuclear: es una cisterna que separa al material genético del citoplasma. Presenta dos membranas separadas por un espacio llamado “cisterna perinuclear”. No es una envoltura continua, sino que esta interrumpida por numerosos poros nucleares que funcionan como sitios de intercambio de moléculas entre el núcleo y el citoplasma. Este tránsito de moléculas, está estrictamente controlado por proteínas ubicadas en dichos poros. Asimismo, la envoltura presenta también ribosomas adheridas al lado citosólico. o Retículo endoplasmático: es un complejo sistema tridimensional de cavidades intercomunicadas, delimitadas por paredes membranosas. Éste, participa en la síntesis, modificación y transporte de moléculas a través de toda la célula. Se divide en 2 tipos: § Retículo endoplasmático rugoso: presenta ribosomas unidos a sus paredes. Transporta y procesa proteínas sintetizadas en sus ribosomas. § Retículo endoplasmático liso: presente SOLO en las células animales (hepáticas, musculares, intestinales, ovarios y testículos). Tiene una apariencia tubular. Realiza la síntesis de lípidos (como triglicéridos o los fosfolípidos), la detoxificación, movilización de la glucosa, y el almacenamiento y liberación de Ca2. Ambos retículos están interconectados, y juntos delimitan un espacio llamado “lumen”, que recorre todo el citosol. o Complejo de Golgi: modifica y distribuye las proteínas y los lípidos, para liberarlas al exterior celular, mediante vesículas de transición y vesículas secretoras. Además, sintetiza hidratos de carbono. o Lisosomas: son pequeñas vesículas dispersas en el citoplasma, que contienen enzimas digestivas de degradación de moléculas complejas. Se originan en el complejo de Golgi. Degradan moléculas incorporadas por la célula, aunque en casos extremos, también pueden degradar organelas para utilizar sus componentes y obtener energía. Cuando una célula muere, la membrana de los lisosomas se rompe y libera hacia el citosol sus enzimas digestivas, que terminan degradando la célula. En las células vegetales y en hongos, la función de los lisosomas es llevada a cabo en gran parte, por su enorme vacuola. • Vacuolas: sacos rodeados de membrana lisa, que contienen el agua dentro del citoplasma. En las células vegetales es una y muy grande, mientras que en las animales son varias y pequeñas. • Centríolos: SÓLO en células animales. Son cilindros proteicos que intervienen en la división celular, cuando se realiza la distribución de los cromosomas a las células hijas. • Citoesqueleto: red tridimensional de proteínas que da forma a la célula, sostiene a las organelas y está asociado al movimiento interno celular. • Pared celular: SÓLO en células vegetales. Está compuesta por celulosa y tiene poros llamados Plasmodesmos. Su función es proteger a la célula. • Microcuerpos: son un grupo heterogéneo de vesículas relacionadas con reacciones de degradación. Su forma suele ser oval o esférica, y están delimitados por una membrana lisa. Se encuentran en el hígado y riñón de los vertebrados, y en las hojas y semillas de las plantas, en las levaduras y en los hongos. EN RESUMEN... CÉLULA VEGETAL CÉLULA ANIMAL Nutrición Autótrofas, con presencia de cloroplastos. Heterótrofa. Carecen de cloroplastos. Pared celular Compuesta por celulosa y otros polisacáridos. Ausente. Vacuola Ocupan aproximadamente el 90% del citoplasma. Escasas y pequeñas. División celular. Cariocinesis sin centriolos ni huso acromáticas en plantas con flor. Citocinesis con placa celular. Cariosinesis con centriolo y huso acromático. Citocinesis por constricción. Plasmodesmos. Presentes. Ausentes. Microcuerpos. Peroxisomas y glioxisomas. Peroxisomas. Según su función y localización, pueden ser peroxisomas (presentes en ambas células), glioxisomas, o hodrogenosomas (presentes SÓLO en células vegetales). 2.6.- Virus, viroides y priones.
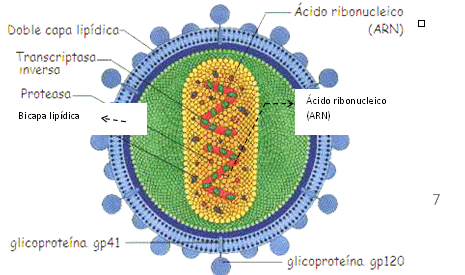
2.6.1.- Virus. Los virus NO son células porque carecen de la compleja red de sistemas imprescindibles para el crecimiento y multiplicación. Tampoco son considerados seres vivos, ya que SIEMPRE dependen, en mayor o menor medida, de la maquinaria celular para sintetizar sus proteínas e incluso para replicarse. Por eso, son parásitos intracelulares obligatorios. Estructura - Composición. Sus estructuras son partículas constituidas por diferentes macromoléculas, como: • Proteínas. • Ácido nucleico (ADN ó ARN), que constituye el genoma de los mismos. • Envoltura de fosfolípidos (en ALGUNOS casos, NO en TODOS). Cada virus es una partícula individual, que recibe el nombre de “Virón”. Los virones son capaces de soportar condiciones ambientales adversas, atravesar la piel u otras barreras del hospedador. De hecho, todos tienen la capacidad de infectar, y en algunos casos, hasta de producir enfermedades. Están formados por una cápside proteica, cuya función es proteger a su genoma, sobre todo cuando esta fuera de la célula. Dicho genoma puede ser ADN o ARN, en versión lineal, circular, simple cadena, doble cadena, parcialmente doble cadena, ó segmentado. En algunos casos incluso, el genoma puede estar asociado a proteínas (Nucleocápisde).
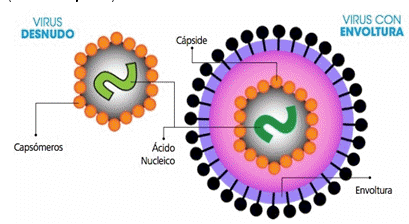
La cápside proteica puede estar recubierta por una bicapa de fosfolípidos con glicoproteínas. Se suelde denominar virus envueltos a aquellos que poseen envoltura, y desnudos a los que carecen de ésta. En algunos casos, la envoltura se encuentra asociada a la nucleocápside, mientras que en otros, se describe un espacio denominado tegumento, que es ocupado por otro conjunto de proteínas. Vías de transmisión. Los virus se transmiten entre los organismos animales, por: • Vía oral-fecal: son diseminados por ingestión de alimento o agua contaminada, y se excretan en las heces o en la orina para continuar con su ciclo. Por ej.: generan gastroenteritis. • Vía respiratoria: se diseminan en forma de aerosol o mucosidades. Como son inestables fuera del cuerpo, el contagio entre personas, se da por la distancia que tienen entre sí (cuanto más cerca, más posibilidad de contagio). Estos, producen enfermedades respiratorias, que pueden infectar otros sistemas. • Vía sanguínea: podemos encontrar virus que se transmiten por un vector (artrópodos hematógafos) como el virus del Dengue, y otros, que se transmiten por exposición a sangre contaminada u otros fluidos corporales, como el VIH-Sida, Hepatitis B o C. • Fluídos corporales y/ó vía sexual: aquellos que se transmiten por contacto directo, ya sea saliva, sudor, semen, o secreciones vaginales. Por ejemplo: virus del Herpes de tipo 1 y 2, el de VPH o HPV (Papilomavirus humano), VIH, y/ó Hepatitis B. • Infección congénita: las madres contagian a sus hijos ya sea a través del útero, o por el pasaje del canal de parto. Entre los más conocidos, encontramos los virus responsables del VIH, el Citomegalovirus, y el viurs de la Rubéola. • Relación directa con animales: como el virus de la rabia, el gantavirus y el arenavirus. El primero está relacionado con murciélagos y perros, y los dos últimos están asociados a roedores. Existen virus capaces de infectar organismos vegetales, PERO NO son capaces de infectar a células bacterianas o animales. Los virus que afectan a BACTERIAS, se llaman “Bacteriófagos”. Ciclo de infeccioso celular. Es una cadena de eventos que ocurren desde que el virus toma contacto con una célula, hasta que el conjunto de “nuevas” partículas virales (progenie viral) sale de la misma. Este ciclo, es EXCLUSIVO de los bacteriófagos (ciclo lisogénico) y puede dividirse en 5 fases:
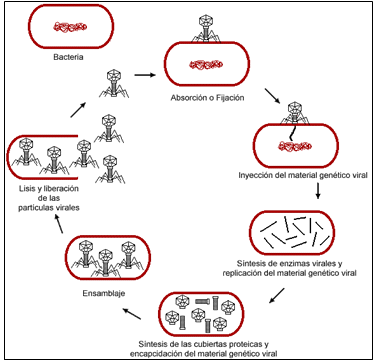
1. Ahesión o adsorción: los virus toman contacto con la célula (la superficie proteica del virus “interactúa” con la superficie proteica de la célula, que actúa como receptora). Las células infectadas por virus, se conocen como tropismos. 2. Penetración: es un proceso que requiere energía, porque los virus usan los mecanismos celulares de transporte de moléculas hacia el citoplasma. Ésta, puede ser: a. Por ingreso del virus completo a través de la membrana. b. Por endocitósis medida por receptor. c. Por fusión de la membrana celular con la envoltura (SÓLO virus envueltos). 3. Desnudamiento: es necesario para que el genoma viral termine de expresar y replicar su cápside. Éste puede ocurrir en 3 niveles: membrana plasmática o endosoma para virus envueltos, o membrana nuclear para virus desnudos. 4. Replicación: todos deben ser capaces de replicar su información genética, y producir sus propias proteínas a través de la traducción molecular. Para ello, utilizan estrategias según el tipo de célula en la que se encuentren: • Si la célula NO posee enzimas para producir ARNm, entonces los virus deberán traducir directamente su genoma, o llevar consigo una enzima que pueda hacerlo. • Si las células NO pueden replicar ADN en el citoplasma, entonces los virus ADN se replicarán en el núcleo utilizando la maquinaria celular para generar ARNm. • Si las células tienen sus propios ARNm, los virus deberán desarrollar alguna estrategia que desvíe la traducción de las proteínas a su favor. 5. Ensamblaje, egreso y maduración: las proteínas virales ya sintetizadas en el citoplasma, utilizan la vía secretora celular para viajar hasta el lugar donde se unirán con el ácido nucleico vial, pasando por varias transformaciones. 2.6.2.- Agentes infecciosos inusuales. Son aquellos agentes infecciosos que no “encajan” en la taxonomía de los virus, y tienen una clasificación a parte. Viroides. Son agentes infecciosos más pequeños, causantes de enfermedades con gran importancia económica, pues se encuentran en las plantaciones de vegetales y cereales del campo. Actualmente se conocen 40 especies distintas, que infectan a las plantas. Están constituidos por una sola cadena de ARN circular de unos 240 a 400 nucleótidos, que se pliega sobre sí misma y no codifica para ningún gen en particular. Tampoco poseen cápside ni envoltura. Los viroides logran propagarse aprovechando el proceso de reproducción vegetativa de algunas plantas, a partir de tubérculos y gajos. En otros casos, se transmiten a través de las semillas, o por daños accidentales en los tejidos. Estos, NO necesitan de una molécula receptora para infectar, y al mutar su molécula de ARN, conforman poblaciones con secuencias de ARN heterogéneas (cuasiespecies). Priones. Son proteínas denominadas PrP. Su forma infecciosa (PrPsc) consiste en acumularse en las neuronas, hasta hacer estallar la célula. O sea que, se expresan en el cerebro, y por algún motivo desconocido, se transforman en agentes patógenos. Cuando éste ingresa al organismo, puede convertir las proteínas priónicas normales, en patógenas, para formar que éstas se multipliquen. A partir de aquí, los pirones tienden a amontonarse y formar estructuras compactas, insolubles en agua y resistentes a proteasas. No obstante, sus estructuras son sensibles a la urea, fenol, e hipoclorito de sodio. A diferencia de los virus, no son reconocidos como “extraños”, y por lo tanto, no desencadenan una respuesta inflamatoria ni inmune a los anticuerpos. Su periodo de incubación es largo, y son específicos según la especie que afecten. Hay 3 formas de enfermedades producidas por priones: una es la esporádica (aparece sin causa aparente); otra es la forma infecciosa (consecuencia de la interacción PrPSc sobre la PrP, ya que la transforma en PrPSc); y la 3ª es la forma hereditaria ( la provocan las alteraciones genéticas, facilitando su plegamiento). CAPÍTULO 3:
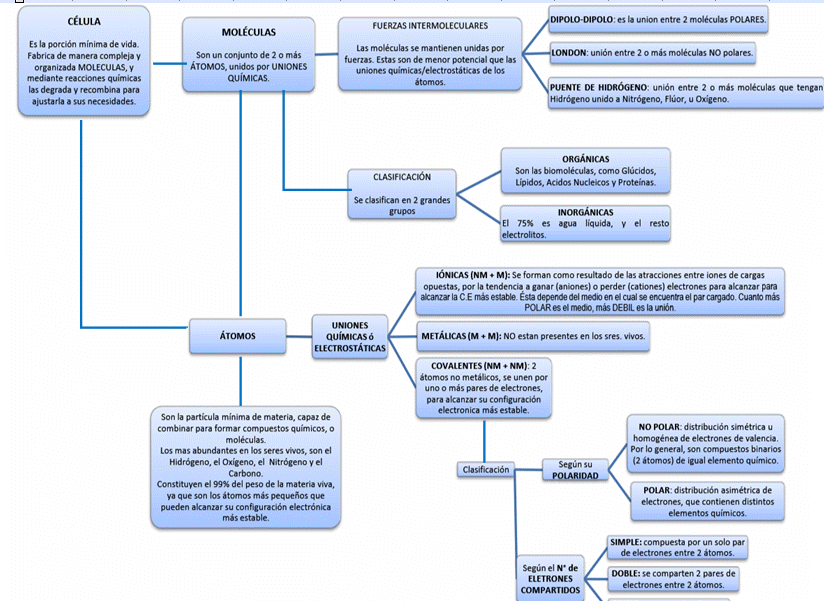

Organización molecular de la célula. 3.1.- Aplicación de los principios de organización de átomos, elementos y compuestos químicos, para la comprensión de las biomoléculas. 3.2.- Naturaleza de las moléculas biológicas. 3.2.1.- Átomo de Carbono. • Es el pilar de la química orgánica y la química biológica. Todas las moléculas organizadas alrededor del átomo de C, constituyen los compuestos orgánicos. • Se puede unir a otros átomos de C, a través de enlaces covalentes simples, dobles y/ó triples, formando largas cadenas (alcanos, alquenos, alquinos, respectivamente). Esto le confiere una gran versatilidad y posibilidad de participar en la formación de diversos compuestos. • Puede formar 4 tipos de átomos de carbono: primario (si esta unido a otro átomo de C), secundario (si esta unido a 2 átomos de C), terciario (si esta unido a 3 átomos de C), y cuaternario (si esta unido a 4 átomos de C). • Dado su reducido tamaño, forma también uniones covalentes muy fuertes entre átomos de OTROS elementos. Se adhiere principalmente a no metales como H, O, N, Cl, F, P y S, formando distintos grupos funcionales. Grupos Funcionales • Son los encargados de caracterizar a la molécula. • Es el conjunto de átomos que participa en las reacciones químicas. • Se clasifican en Hidrocarburos, Compuestos Oxigenados, y Compuestos Nitrogenados. Los más importantes son los últimos 2. 1. HIDROCARBUROS: o Alcanos: hidrocarburos saturados de cadena abierta. Terminación de la molécula de alcano (-ano). o Alquenos: hidrocarburos insaturados de cadena abierta. Terminación de la molécula de alqueno (-eno) o Alquinos: hidrocarburos insaturados de cadena abierta. La terminación de la molécula de alquino, es (-ino) o Hidrocarburos cíclicos: son derivados de los hidrocarburos (serían cadenas de hidrocarburos cerradas). Todos los átomos del ciclo son carbonos, pero también pueden presentar insaturaciones. Se nombran igual que los hidrocarburos de cadena abierta y, con el mismo número de átomos de carbono, pero anteponiendo el prefijo “ciclo”. Los primeros 4 ya nombrados, NO tienen grupos funcionales, o sea, son átomos de C unidos a otros átomos de C. Se los diferencia por la forma que adopta dicha unión. Alcanos, alquenos y alquinos forman cadenas lineales, y los hidrocarburos cíclicos, forman ciclos cerrados. o Hidrocarburos aromáticos: son hidrocarburos derivados del benceno, con las mismas características que los “hidrocarburos cíclicos” (ver ítem anterior). Tienen como grupo funcional al “arilo” derivado de los carbonilos. Los HIDROCARBUROS unidos a ciertos HALÓGENOS, forman a los derivados halogenados. 2. COMPUESTOS OXIGENADOS: o Alcoholes y fenoles: para la nomenclatura, se usa el sufijo “ol”. Son muy abundantes en los hidratos de carbono. Su grupo funcional es el “hidróxilo” (-OH). o Aldehídos y cetonas: sus sufijos son “al” y “ona” respectivamente. Son muy abundantes en los hidratos de carbono. Su grupo funcional es el “carbonilo” (C=O). o Ácidos/ácidos carboxílicos: son ácidos débiles. En su nomenclatura, llevan el sufijo “oico”. Los encontramos en derivados de hidratos de carbono, en los aminoácidos y proteínas, en los ácidos grasos (lípidos). Su grupo funcional es “carboxilo” (-COOH). o Ésteres: resultan de la unión de un ácido con un alcohol, que forman (además de esteres) agua con el grupo OH del alcohol, y el H del ácido. Los encontramos en los glicéridos (lípidos). Su grupo funcional el “acilo” (-R-CO-) o Éteres: resultan de la unión de un alcohol con otro alcohol. Su grupo funcional es el “alcoxi” (-RO). 3. COMPUESTOS NITROGENADOS: o Aminas: son derivados del amoniaco (NH3). Uno, dos o los tres hidrógenos del NH3 pueden reemplazarse por grupos sustituyentes (las letras R), dando origen a aminas 1as, 2as y 3as respectivamente. Están presentes en los aminoácidos. Su grupo funcional es el “amino” (-NH2 ; -NRH ; NR2). o Amidas: resultan de la reacción entre una amina y un ácido carboxílico (ver cuadro). Están presentes en las uniones peptídicas entre aminoácidos. Su grupo guncional es el “amino” (-NH2 ; -NRH ; NR2) y el “carboxilo (-C=O). 3.2.2.- Molécula de Agua. • Constituye entre el 70 y el 90% de los seres vivos. • Se halla repartida en todo el organismo, pero no se la considera líquido inerte. • Es el solvente en el cual se hallan disueltas o suspendidas las sustancias necesarias para la existencia de las células. • Las estructuras, propiedades y comportamiento de las biomoléculas están influenciadas por ella y sus productos de disociación. Propiedades. o La cohesión y adhesión, es la unión entre moléculas de agua y entre el agua con otras moléculas polares respectivamente. Esta relación, permite a las plantas transportar nutrientes disueltos desde la raíz hasta las hojas por capilaridad. o El alto calor específico del agua: permite a los seres vivos mantener su temperatura constante, aunque cambiemos el entorno. o La baja densidad del hielo con respecto al agua líquida, hace que el hielo flote y los cuerpos de agua se congelen en la superficie. Así, el hielo actúa de aislante, manteniendo constante la temperatura del agua. • Es una molécula polar con distribución asimétrica de los electrones de valencia. Sus fuerzas intermoleculares son dipolo-dipolo permanente, y sus átomos se unen por puente de hidrógeno, aunque EN ESTE CASO, sean más débiles que las uniones covalentes. Solubilidad.
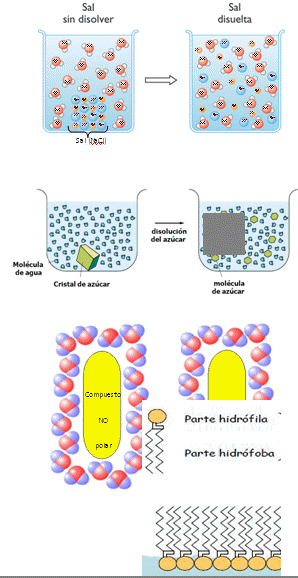
• Agua + compuesto IÓNICO = SOLUCIÓN IÓNICA. Los compuestos iónicos son solubles en agua. Cuando se disuelve cualquiera de ellos en agua, las fuerzas entre el solvente y los iones positivos y negativos, son más fuertes que los que mantienen unidos a los iones en el cristal. Por eso, el cristal se disuelve, y los iones se rodean de una capa de dipolos de agua, formando una solución iónica. • Agua + compuesto POLAR = SUSTANCIA MOLECULAR. SÓLO son solubles en agua aquellos compuestos polares que, al unirse con ésta, formen puentes de hidrógeno con sus moléculas. Por ejemplo, al disolver glucosa en agua, las moléculas se separan y se unen a las moléculas de agua, y se rodean de un dipolo permanente mediante puentes de hidrógeno, formando entonces una solución molecular. • Agua + compuestos NO polares = INTERACCIÓN HIDROFÓBICA. Es IMPOSIBLE que una molécula NO polar se disuelva en agua, ya que éstas son incapaces de establecer enlaces puente de hidrógeno. Por lo tanto, no se crean sustancias, sino INTERACCIONES HIDROFÓBICAS. Las interacciones hidrofóbicas son importantes en la estabilización de la estructura de proteínas y ácidos nucleicos, en las interacciones moleculares de los sistemas biológicos (enzima-sustrato, antígeno-anticuerpo), y en la formación de estructuras subcelulares como las membranas. • Agua + moléculas POLARES + moléculas NO polares = SUSTANCIA ANFIPÁTICA/ ANFÍLICA. Cada grupo carboxilo del compuesto polar, puede establecer puentes de hidrógeno con el agua, formando cabezas hidrofílicas. Pero los compuestos no polares en cambio, tienen a unir sus colas hidrocarbonadas no polares a otras colas hidrofóbicas de moléculas similares, por acción de las interacciones hidrofóbicas. Éstos se mantienen agregados por fuerzas de Van der Waals. Como consecuencia de este doble comportamiento, se forman micelas en el agua (por ejemplo las micelas de jabón), en las que grupos carboxilos negativos (cabezas hidrofílicas) están en contacto con el agua, y los grupos NO polares (colas hidrófobas//hidrofóbicas) permanecen ocultos dentro de la estructura micelar, la cual NO está en contacto con el agua por las fuerzas de repulsión que ejerce con ésta. 3.2.3.- Las biomoléculas. TODOS los seres vivos están compuestos de 4 clases de biomoléculas: • Lípidos: constituyen una gran variedad de sustancias con la característica común de ser insolubles en solventes polares (el agua por ej.). • Proteínas: hay varios miles diferentes, todas formadas por los mismos 20 aminoácidos (monómero). • Ácidos nucleicos: son los responsables de nuestra identidad, y son el resultado de una combinación en largas cadenas de 4 nucleótidos (monómero) diferentes. 3.3.- Carbohidratos. Definición. Son todos derivados de los monosacáridos (monómero). Son sustancias que tienen en común los grupos funcionales como aldehídos o centonas, y alcoholes. Importancia. • 3 compuestos más abundantes de la biósfera (celulosa, quitina y almidón) pertenecen a los glúcidos. • Son el combustible energético de la célula (glucosa). • Tienen función energética y estructural: la celulosa conforma las paredes celulares de los vegetales; la quitina es el componente fundamental del exoesqueleto de los artrópodos; y el almidón funciona como reserva energética de los vegetales, al igual que el glucógeno en los animales. Rol fundamental. Aportan una considerable parte de la energía necesaria para cubrir las necesidades metabólicas en células procariotas y eucariotas. Estructura química. Su formula general es C¬n(H2O)n para n ≥ 3. Sin embargo, pueden estar unidos a más grupos funcionales. 3.3.1.- Monosacáridos. Características generales. Su formula general es C¬n(H2O)n para n 7 ≥ 3 (porque tienen de 3 a 7 carbonos). Deben ser aldehídos o centonas con más de una función alcohol, ubicados en carbonos diferentes. El más pequeño estará formado por 3 carbonos, llamándose “triosa”. Uno de sus C (el 1°) para la función del aldehído, ó el segundo C para una cetona. Los otros dos contienen alcoholes en cada uno de ellos. Según la cantidad de carbonos se denominan “tri”, “tetro”, “pento”, “hexo” o “heptosas” (de 3 a 7 respectivamente) • Las tetrosas (4 C) cumplen un rol esencial en el proceso de la fotosíntesis (fase oscura), y en el ser humano u otros vertebrados que participan en la vía metabólica del “ciclo de las pentosas”. • Pentosas (5 C): entre las más importantes tenemos la D-ribosa y sus derivados (desoxirribosa, ribosa 5 fosfato, etc.) que están presentes en vegetales y bacterias; la xilosa que interviene en la estructura de los proteoglucanos; y la D-Ribulosa que interviene en la fotosíntesis, y es la precursora de la fructosa. Poseen isomería óptica: tienen un C asimétrico (unido a cosas distintas o polares). Gracias a esta propiedad, desvían la luz polarizada, ya sea a la derecha (dextrógiros) o la la izquierda (levógiros). Derivados. • Alcoholes: se reduce el grupo carbonilo (C=O). Que se reduzca significa que hay menos O y más H. • Ácidos: se dan por oxidación de la glucosa. Sí es suave dicha oxidación, se llama ácido glucónico; sí la oxidación se produce en el C1 y el C6, se llama ácido glucárico; y si se produce sólo en el C6, se llama glucurónico. • Ésteres: se forman por reacción de OH- con ácido fosfórico. • Aminoazúcares: se reemplaza un OH- por un grupo amino (NH2). • Desoxiazúcares: monosacáridos que pierden un OH-. 3.3.2.- Disacáridos. Resultan de la unión de dos monosacáridos, con pérdida de una molécula de agua. La condensación de estos, se verifica entre el oxhidrilo del carbono anomérico de un monosacáridos, y un oxhidrilo alcohólico cualquiera de otro monosacáridos. Su unión se la denomina glucosídica (caso particular de unión éter), y puede ser α ó β. R - OH (anomérico) + OH - R (cualquiera) R - O - R’ (unión glucosídica) + H2O (agua) Casi todos los disacáridos tienen poder reductor, dado que el segundo azúcar (a la derecha de la formula) tiene su carbono anomérico libre. La sacarosa es la excepción, pues la unión que tiene se hace con oxhidrilos de dos carbonos anoméricos. Entre los disacáridos más importantes, se encuentran: maltosa, isomaltosa y celobiosa (formadas las 3 por 2 moléculas de glucosa), lactosa (galactosa + glucosa) y sacarosa (glucosa + fructosa). 1) Oligosacáridos. Resultan de la unión de más de 2 monosacáridos, y hasta un máximo de 20. Los de mayor interés biológico son aquellos relacionados con proteínas (glucoproteínas), compuestos que resultan de una elaborada expresión génica. La fracción glucídica de éstos, se asocia a funciones de reconocimiento y señalización celular; por ésta razón son abundantes en las membranas biológicas (glucolípidos) y en las moléculas del sistema inmunitario (inmunoglobinas). Por ejemplo, el reconocimiento de los grupos sanguíneos. La función de reconocimiento y señalización no consiste solamente en diferenciar lo propio de lo ajeno, sino que los organismos pluricelulares, también sirve como guía en los procesos de migración celular y en la distribución de biomoléculas entre los distintos tejidos, todo lo cual presupone una alta variabilidad estructural. Sus unidades estructurales entonces, presentan numerosos puntos reactivos (alcoholes) de los cuales no solo pueden proyectarse por encima y por debajo del plano de la molécula (isomería, epimería, anomería), sino que además muestran diversos sustituyentes (por animación, fosforilación, oxidación, sulfatación, metilación) y más aún, pueden formar cadenas ramificadas. 3.3.3.- Polisacáridos. La forma predominante de los glúcidos en la naturaleza, es como polisacáridos. Los polisacáridos son polímeros de alto peso molecular que por hidrólisis enzimática o ácida, dan unidades de monosacáridos. No tienen sabor dulce como los monosacáridos, y dado su gran paso molecular, cuando son solubles dan soluciones coloidales. Tampoco tienen poder reductor, debido a que las uniones glicosídicas que los conforman impiden la formación de enodioles, encargados de dicho poder. Los polisacáridos se dividen en: • Homo-poli-sacáridos: por hidrólisis dan un solo tipo de monosacárido, como almidón, glucógeno, celulosa, y/ó insulina. • hetero-poli-sacáridos: por hidrólisis dan distintos tipos de monosacáridos como los glucos-amino-glucanos. A. Homo-poli-sacáridos. • Están formados por la repetición de un monosacárido. • Tienen funciones estructurales, como la celulosa y la quitina; o bien, de reserva como el almidón y glucógeno. à Almidón. Es la forma bajo las cuales las células vegetales almacenan la glucosa, formando gránulos. Está compuesto por dos porciones: amilosa y amilopectina, ambas son polímero de la glucosa, pero presentan una estructura espacial distinta. La amilosa tiene estructura no ramificada helicoidal, mientras que la amilopectina es ramificada. à Glucógeno. • Polisacárido de reserva en animales (equivalente al almidón de las células vegetales). • Se almacena en el hígado y en el músculo. • Es la principal fuente de glucosa endógena. • Es la primera reserva de energía que se utiliza durante el ayuno à Celulosa. • Polisacárido más abundante de la naturaleza. • Está presente en la pared celular en las plantas. • Es un polímero lineal de celobiosa( glu-gluβ1,4), • Forma fibrillas. • No se hidroliza (no la podemos digerir), pero a la vez, favorece los movimientos peristálticos del intestino (fibra de la dieta) • Insoluble en agua, álcalis y ácidos diluidos. • Absorbe sales biliares y colesterol. à Quitina. • Polímero lineal, cuyo eslabón básico es β-D N-acetilglucosmina. • Sus funciones son las mimas que las d las celulosa, pero ésta se encuentra en moluscos y antrópodos, más precisamente sobre el exoesqueleto. • Cumple funciones de almacenamiento intracelular como el almidón y el glucógeno. • Forma cintas, por los enlaces α-glucosídicos. B. Hetero-poli-sacáridos. Formados por la repetición de un disacárido. à Glucosaminoglicanos (GAG). • Son los más abundantes del cuerpo. • Forman cadenas lineales no ramificadas, cuyos eslabones son repetitivos. • Son extracelulares (se encuentran en la matriz extracelular de los animales). • La unión glucosídica que liga una unidad repetitiva con otra, se llama interdimérica. La unión glucosídica que vincula dos componentes de UNA unidad repetitiva entre sí, se llama intradimérica. • Contiene grupos sulfato (SO4) en su estructura. Cuanto más sulfato tienen, más negativos se tornan. • Atraen cationes como Na+, Ca+2, y H2O. • Están unidos a proteoglicanos (sino, se repelan). • Se encargan de lubricar articulaciones y regular la hidratación celular y tisular. àPeptidoglucanos. • Presente en paredes de las bacterias. • Glicos-amino-glicanos unidos a una proteína central (core proteico.) • Es una cadena lineal unida por péptidos pequeños. • La penicilina inhibe la síntesis de peptidoglucanos. • La enzimalisozima (saliva) hidroliza estas uniones β-glicosídicas. 3.4.- Lípidos. Son una serie heterogénea de compuestos que tienen en común una propiedad física: son poco solubles o insolubles en agua, pero solubles en solventes no polares. Se dividen en saponificables e insaponificables, según su capacidad para formar jabones. 3.4.1.- Saponificables. • Contienen por lo menos un ácido graso en su estructura. • Su unión es de tipo éster, la cual une un alcohol con un ácido graso. • NO forman polímeros. • Aquellos de gran importancia biológica son: los que tienen un alcohol (acil-gliceridos), o bien glicerol no nitrogenado (fosfo-acil-glicéridos), o bien esfingol nitrogenado (esfingol-lípidos). A. Ácidos grasos. • Fórmula general: CH3 –(CH2)n – COOH ó . • Son largas cadenas hidrocarbonadas con un grupo carboxilo (-COOH). • Los más importantes tienen 16 y 18 carbonos (siempre tienen números pares). à Clasificación. Se clasifican en saturados/insaturados, y en esenciales/no esenciales. • Saturados: NO tienen doble ligadura entre ningún C. • Insaturados/enoicos): poseen doble ligadura. Sí solo tienen una doble ligadura, son mono-enoicos; PERO sí tienen más, son polienoicos. Los de gran importancia biológica tienen configuración geométrica cis (producen curvatura en la cadena). Entre los más destacados, encontramos los aceites omega (3, 5, 6, 8, 9, 11, y 14). • Esenciales: son los que no podemos sintetizar y por lo tanto debemos incorporar con los alimentos. Son los AG polienoicos(series Ɯ3y Ɯ6) • NO esenciales: los sintetizamos nosotros mismos. Son los ácidos saturados y mono-enoicos. à Propiedades. • Son ácidos débiles. • A pH fisiológico (7,35) el grupo carboxilo está ionizado (COO-) • A mayor longitud de la cadena, mayor T° de fusión y menor solubilidad en agua. • A mayor n° de dobles ligaduras, menor punto de fusión. • Son moléculas ANFIPATICAS. Se componen de una cabeza polar (correspondiente al grupo carboxilo) afín con el agua (hidrófila), y una cola NO polar (correspondiente a la parte hidrocarbonada) marcadamente hidrofóbica. • En solución acuosa forman MICELAS, dejando las colas hacia adentro, y las cabezas hacia afuera para que estén en contacto con el agua. • A T° ambiente son líquidos sólo aquellos ácidos grasos que tengan 10 átomos de C o menos. Las cadenas más largas, son sólidas. • Las grasas de origen vegetal y animal son ricas en ácidos grasos esterificados, y muchas de ellas son insaturadas. B. Acilglicéridos • Son ésteres del glicerol con ácidos grasos (saturados o no saturados). • Pueden ser mono, di o triglicéridos, dependiendo de la cantidad de moléculas de ácidos grasos que tenga. • Son los más abundantes en la naturaleza. • Rol fundamental: reservar energía en el citoplasma, gracias a que son insolubles en agua, osmóticamente inactivos (no atraen el agua), y altamente calóricos (proporcionan el doble de calorías que los HdC) • Son excelentes aislantes térmicos. • Se almacena en el tejido adiposo. • Son excelente combustible para la célula cuando se hidrolizan. • En animales, son las grasas (grasas saturadas) mientras que en vegetales son los aceites (grasas insaturados). • Saponificación: sí a un triglicérido se lo trata con KOH o NaOH en caliente, se rompe el enlace éster y se forma 1 molécula de glicerol y 3 moléculas de jabón (el ácido graso reemplaza al H por el catión K+ o Na+). o Al esterificarse los alcoholes del glicerol, los A.G pierden su afindidad con el agua, y los glicéridos (en especial triglicéridos) son muy pocos solubles en ese solvente polar. o Si los A.G que esterifican al glicerol son saturados, el glicérido resultante será sólido a T° ambiente (grasa). No obstante, si los A.G son insaturados, el glicerol será líquido (aceite). C. Fosfoacilglicéridos à Estructura. Glicerol + 2 ácidos grasos + ácido fosfórico + grupo polar (puede ser colina - etanolamina - serina - inositol). Se caracterizan por poseer una unión éster en el C3, con el ácido fosfórico, mientras que en C1 y C2, los ésteres son con ácidos grasos (en C1 saturados y en C2 insaturados). à Comportamiento en H2O. •
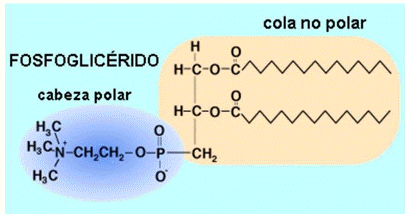
Son anfipáticos (cabeza polar y dos colas no polares) y en medios acuosos forman bicapas. à Función. • Estructural: son los principales constituyentes de las membranas biológicas. • Se distribución asimétricamente en éstas. o Fosfatidilcolina: predomina en cara externa. o Fosfatidilserina y fosfatidiletanolamina: predominan en cara interna. o Fosfatidilinositol: en ambas caras. D. Esfingolípidos
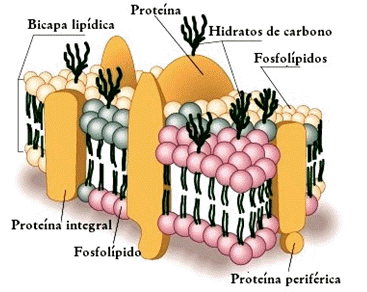
à Estructura Molécula de 18 carbonos: tiene alcohol primario, grupo amino en el C2, alcohol secundario en el C3, y doble ligadura entre los carbonos 4 y 5; el resto son cadenas de hidrocarburos alifáticas ESFINGOL + AG CERAMIDA (aminoalcoholde C18) CERAMIDA + GRUPO POLAR ESFINGOLIPIDO Se asocia a ácidos grasos, a través de una amida con el N del C2, conformando ceramida. à Clasificación. Según el grupo polar unido a la ceramida, se denominan: • Gangliósidos: glucolípido que tiene oligosacáridos como grupo polar. • Cerebrósidos: glucolípido que tiene monosacáridos como grupo polar. • Esfingomielina: fosfolípido que tiene como grupo polar a la fosforilcolina. à Funciones. • Son moléculas anfipáticas. • Se encuentran en la matriz lipídica de las membranas biológicas, y también la capa externa de la membrana plasmática pero en menor cantidad que los fosfo-acilglicéridos. • En ésta, también se encuentran esfingoles unidos covalentemente con glúcidos, constituyendo la glucocaliz (rol fundamental en el reconocimiento entre células). • Suelen estar en el tejido nervioso. 3.4.2.- Insaponificables. • No contienen AG en su estructura. • Derivan de un hidrocarburo de C5, el “isopreno”. • Se clasifican en Terpenos y Esteroides. A. Trepenos. • Formados por dos o más unidades de isopreno, unidos por una “ordenación cabeza-cola”. • Pueden ser lineales, cíclicos o mixtos. • Se encuentran fundidos en los pigmentos y escancias verdes de las plantas (clorofila, carotenos, limoneno), ó bien, en la coenzima Q (cadena respiratoria) de los animales, donde actúa como precursor de vitaminas A, E y K. • Está asociado a la matriz lipídica de las membranas, por su carácter hidrofóbico. B. Esteroides. • Son derivados cíclicos del isopreno. • Tienen un núcleo hidrocarbonado formado por 4 anillos. 3 de ellos son ciclohexanos, y el 4° es ciclopentano. • De este compuesto derivan los esteroles, de los cuales el COLESTEROL es el más importante en los tejidos animales. COLESTEROL • Molécula hidrofóbica con leve carácter polar. • Muy abundante en las membranas de las células eucariotas animales (regula la fluidez de las membranas). • Las membranas de las células vegetalesNO TIENEN COLESTEROL, tienen un derivado que es el ergosterol. • Función: es el precursor de numerosos compuestos de importancia biológica. Por ejemplo: hormonas sexuales (andrógenos y estrógenos), progesteronas, gluco-corticoides, mineralocorticoides, vitamina D, sales biliares, membrana plasmática, etc. 3.5.- Aminoácidos y Proteínas. 3.5.1.- Aminoácidos.
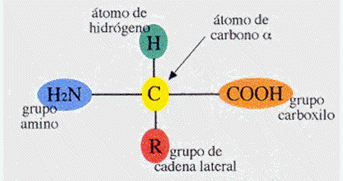
• Son las unidades estructurales de las proteínas. • Se abrevian AA. • Su fórmula general es: • 20 AA diferentes forman las proteínas Se diferencian en la cadena lateral ®. Propiedades ácido - base. • Los AA pueden comportarse como ácidos (ceder H+) o como bases (captar H+) según el pH del medio en el que se encuentran. • A pH fisiológico se encuentran como iones DIPOLARES. Clasificación. De acuerdo a la naturaleza de la cadena lateral ®: • AA con R NO polar. • AA con R polar sin carga. • AA con R polar con carga positiva (AA básicos). • AA con R polar con carga negativa (AA ácidos). Unión peptídica = unión amina. • Se forma por la condensación entre el grupo α-carboxilo de un AA y el grupo α-amino de otro. • Tiene cierto carácter de doble ligadura. • Es plana y rígida. • Su configuración isomérica es TRANS. • Según el N° de AA unidos por uniones peptídicas: dipéptidos, poliéptidos, proteínas. 3.5.2.- Proteínas. Funciones. • Protección (queratina). • Soporte mecánico (colágeno). • Catálisis (enzimas). • Transporte: a través de membranas (canales, carriers, bombas) y por el torrente sanguíneo (albúmina, hemoglobina, etc.). • Hormonas (insulina, glucagón). • Receptores para hormonas y neurotransmisores. • Defensa (inmunoglobulinas). • Factores de la coagulación sanguínea. • Contracción muscular (actina, miosina). Niveles de organización estructural. Los AA que forman las proteínas se unen entre sí formando cadenas lineales no ramificadas. Estas cadenas luego se van organizando en el espacio adoptando diferentes estructuras tridimensionales. Solo cuando la proteína complete su organización espacial adquirirá ACTIVIDAD BIOLOGICA. 1. Estructura primaria:
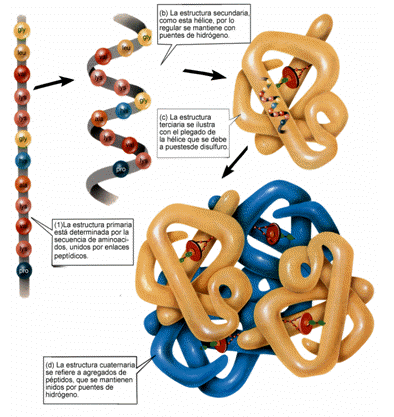
• Describe el número, clase y secuencia de aminoácidos que constituyen a la proteína. • Esta sostenida por enlaces covalentes (uniones peptídicas y puentes disulfuro). • Es la estructura que le da identidad biológica a la proteína. 2. Estructura secundaria: organización espacial de la estructura primaria. Está estabilizada por uniones Puente de Hidrógeno entre todos los α-NH2 y α-COOH. Puede generar 4 tipos de formas distintas: a) a-helice: tiene 3,6 AA por vuelta. Conforman una estructura en forma de bastón, donde la cadena polipeptídica se enrolla alrededor de su eje, formando una estructura helicoidal. Sus puentes de H se dan entre el α-C=O de cada AA y el α-NH del 3°que le sigue en la secuencia. Son uniones intracatenarias, paralelas a la hélice. Los R quedan en la parte exterior de ésta. El AA Pro (Prolina) desestabiliza dicha estructura, y la forma de una manera distinta. b) β-conformacion(hoja plegada): los puentes de H se dan entre α-C=O y α-NH de la misma cadena (intracatenarios) o de cadenas diferentes (intercatenarios). Los R se orientan haca arriba o hacia abajo del plano de la hoja plegada. c) Triple hélice (colágeno). d) Super-secundaria (mixta): son estructuras secundarias mixtas donde se combinan zonas de α-helice, zonas de hoja plegada y zonas random(al azar, sin patrón definido). 3. Estructura terciaria: plegamiento de la estructura secundaria. • Pueden ser proteínas fibrosas (estructura fibrilar, alargada) o, proteínas globulares (estructura esferoidal). • Se unen mediante interacciones hidrofóbicas, uniones Van der Waals, puentes de hidrógeno, e interacciones salinas. 4. Estructura Cuaternaria: sólo está presente en proteínas multiméricas (más de una cadena polipeptídica). Cada una de las cadenas se denomina Subunidad o Proomero. Las subunidades pueden ser iguales, similares o distintas. Se estabilizan por medio de uniones débiles (interacciones hidrofóbicas, PdH, interacciones salinas y de Van der Waals). Desnaturalización e Hidrólisis.
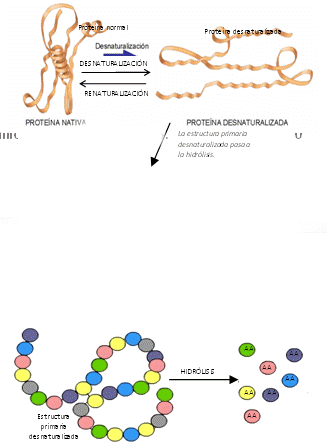
A temperaturas entre los 50 ºC y los 80 ºC TODAS las proteínas se desnaturalizan, es decir pierden sus estructuras 2º, 3º y 4º, PERO muchas veces, conservan su estructura 1ª. Así, las uniones débiles se rompen y PIERDE SU FUNCIÓN BIOLÓGICA. Sin embargo, esto se podría revertir si es muy reciente la desnaturalización, o bien, conservar en su estructura primaria (desnaturalizada). En casos más severos, la proteína desnaturalizada puede sufrir la hidrolización de su estructura primaria. En cuyo caso, se pierden todo tipo de uniones, y el resultado serán sólo aminoácidos (AA) dispersos. También quedan sin actividad biológica, pero éste proceso ya NO es reversible. Proteínas conjugadas. Son proteínas con grupos prostéticos, no peptídicos, unidos mediante enlaces covalentes, a las partes peptídicas de la misma (apoproteína). Las mismas NO funcionan si alguna de las partes anteriores no está presente. Asimismo, se las puede clasificar de acuerdo a su grupo prostético: CLASE DE PROTEÍNA GRUPO PROSTÉTICO (componente no proteico) EJEMPLOS Glicoproteínas Glúcidos (una o más cadenas de monosacáridos). Inmunoglobulinas, mucinas, proteínas de membrana. Lipoproteínas Fosfolípidos, ácidos grasos, lípidos neutros. Quilomicrones, rodopsma. Nucleoproteínas Ácidos nucleicos Proteínas víricas. Metaloproteínas Metales o iones metálicos Ferritina, carboxipeptidasa. Hemoproteínas Hemo Mioflobina, hemoglobina, citocromos. Flavoproteínas Derivados vitamínicos. Enzimas de oxido-reducción. Hemoglobina y mioglobina. A. Hemoglobina (Hb). Es la encargada de transportar oxígeno por el torrente sanguíneo, desde los pulmones hacia los tejidos, y viceversa. Asimismo, es capaz de regular el pH sanguíneo. • Molécula tetramétrica: 4 globinas de las cuales, son 2 α y 2 β, c/u con un bolsillo para el hemo. • Tiene estructura cuaternaria • El bolsillo hidrofóbico “homo” impide que el Fe++se oxide a Fe+++. • Cada molécula de Hb transporta 4 moléculas de O2. • Tiene menor afinidad por el O2 que la Mb. La Hb es una proteína alostérica, que tiene 3 moduladores alostéricos negativos: el H+ (efecto Bohr), el CO2, y el BPG (bisfosfoglicerato). Éstos, se unen a la Hb en diferente sitio que el O2, disminuyendo su afinidad por el oxígeno, y favoreciendo a la vez, la descarga de la Hb. Asimismo, tiene un efecto cooperativo, lo que significa la unión de un hemo con el O2. La Hb en estado tenso, muy unida, facilita esta acción a los 3 hemos restantes, y pasa al estado relajado, aumentando la afinidad de éstas subunidades por el O2. B. Mioglobina
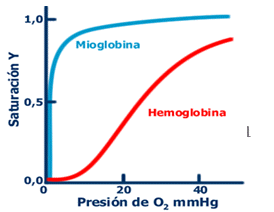
(Mb). La mioglobina (en el músculo) almacena O2 y lo libera a la mitocondria para la respiración celular. • Molécula monomérica (una sola globulina con un sólo grupo hemo). Sin embargo, las subunidades de la Hb y la única de la Mb son iguales. • Tiene estructura terciaria. • Cada molécula de Mb, trasporta una molécula de O2. à Curvas de saturación de Hb y Mb. • Hb y Mb se unen reversiblemente al O2. Sin embargo, Hb tiene menor afinidad por el O2 (curva sigmoidea, p50 mayor) que la Mb (curva hiperbólica, p50 menor). • P50= presión parcial de O2, a la cual el 50% de los grupos hemo están unidos al O2. Colágeno. • Es una proteína fibrosa presente en los animales. • Son las proteínas más abundantes de los vertebrados. • Poseen gran resistencia mecánica y son inflexibles. • Principal componente de piel, huesos, cartílagos, tendones y dientes. • Su estructura primaria es atípica, ya que responde a la estructura Gly (glicina)-X-Y, donde X e Y suelen ser hidroxiprolina e hidroxilisina. Estas últimas dos son exclusivas del colágeno. Siempre cada 2 AA aparece la glicina, constituyendo un tercio de la proteína. • La molécula del colágeno, el Tropocolágeno, está formada por 3 cadenas polipeptídicas, que pueden ser o no iguales pero siempre manteniendo la estructura Gly-X-Y. • La estructura secundaria del colágeno es de Triple hélice, y es exclusiva de este. Las moléculas de tropocolágeno se asocian formando fibrillas y fibras. 3.6.- Nucleótidos y ácidos nucleicos. 3.6.1.- Nucleótidos. à Funciones: • Monómeros de los ácidos nucleicos (ADN y ARN) • Transferencia de energía (ATP). • Segundos mensajeros de ciertas señales químicas. • Activadores de moléculas en procesos de biosíntesis de lípidos, proteínas e hidratos de carbono. • Coenzimas (NAD+, FAD, etc). à Estructura: BASE NITROGENADA + PENTOSA + PO4H3 NUCLEOSIDO • La pentosa puede ser de 2 tipos: • Las bases nitrogenadas son de 2 tipos distintos: púricas (como la adenina y la guanina) y piramídicas (como la timina, citosina y uracilo). à Nucleósidos. La pentosa se une a la base nitrogenada, por medio de una unión covalente de tipo β-N-glucosídica entre el HO del C1’de la pentosa y un N de la base nitrogenada. Asimismo, la unión entre nucleótidos es un enlace fosfodiester: el fosfato 5’de un nucleótido se une al HO 3’de otro nucleótido formando un puente fosfodiester. 3.6.2.- Ácidos nucleicos. ADN. • Molécula con dos cadenas polinucleotídicas. • Sus bases nitrogenadas son: adenina, citosina, timina, y guanina. • Su pentosa es: la desoxirribosa. • Sus nucleótidos se unen por medio de enlaces fosfodiester. • Las cadenas son antiparalelas y complementarias: o Antiparalelas porque una de las cadenas se orienta en dirección 5’ ---> 3’, mientras que la otra en dirección opuesta. o Complementaria porque las bases se combinan de a pares (Púrica + Piramídica): la Adenina se une por medio de 2 Puentes de Hidrógeno con la Timina; y la Guanina, que se une a la Citosina por medio de 3 Puentes de Hidrógeno. • Por su conformación helicoidal, la molécula de ADN presenta surcos mayor y menor. • El número de A es igual al de T, y el número de G igual al de C. ARN. • Molécula monocatenaria (1 sola cadena). • Sus bases nitrogenadas son: adenina, guanina, citosina, y uracilo. • Su pentosa es la Ribosa. • Los nucleótidos se unen por medio de enlaces fosfodiester. • Existen 5 tipos de ARN: ARNm (mensajero), ARNr (ribosomal), ARNt (de transferencia), ARNn (pequeño nuclear, presente sólo en eucariotas), y ARNc (pequeño citoplasmático, presente sólo en eucariotas). • Son más pequeños que el ADN. CAPÍTULO 4: Introducción al metabolismo. 4.1.- Bioenergética. ENERGIA: capacidad de realizar trabajo. • Los seres vivos necesitan energía. • La principal fuente de energía de los seres vivos, es el Sol. • Ésta, solo se observa a través de sus transformaciones, que producen un efecto. • Los seres vivos obtienen la energía del alimento, el cual funciona como combustible. BIOENERGÉTICA: transformaciones y cambios que sufre la energía con la que los seres vivos sostienen de orden molecular. 4.2.- Transformaciones de energía en los seres vivos. • La célula es un sistema que extrae energía del medio. • Convierte la energía en trabajo, con una eficacia superior al de las máquinas humanas. • Las estructuras de transformación están constituidas por moléculas orgánicas frágiles. • La energía que toma del entorno, se acumula en forma de: o Energía química. Está contenida en los enlaces químicos entre átomos. Esta forma es característica de las células autótrofas fotosintéticas. Ingresa a ésta a través la clorofila, que capta la energía lumínica de los rayos de Sol, y la transforma en energía química para distintos trabajos posteriores. o Trabajos osmóticos (transporte de materiales hacia el interior de la célula). o Trabajos mecánicos (contracción muscular, locomoción, etc.). 4.3.- Consideraciones generales sobre la termodinámica de los seres vivos.
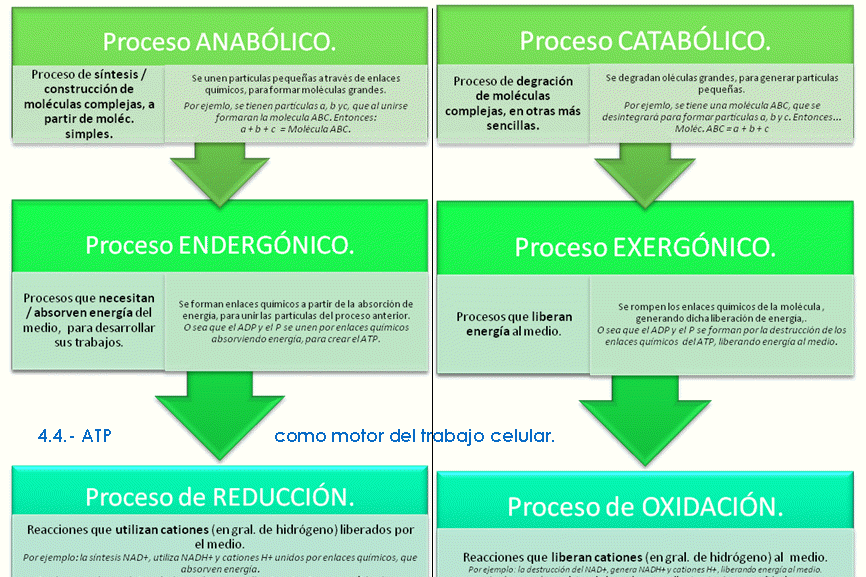
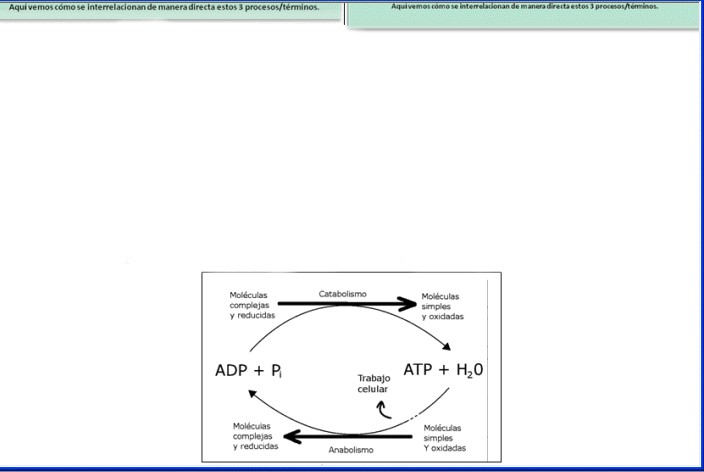
4.4.- ATP como motor del trabajo celular. • Papel central en el metabolismo de las células. • Estructura: 3 grupos fosfato + Ribosa + Purina (Adenina). • Es el intermediario energético entre los procesos anabólicos y catabólicos. El enlace entre el 2º y 3er grupo fosfato, es muy rico en energía, por lo tanto, necesita de mucha energía para establecerse, y a su vez, también libera mucha energía cuando éste se rompe. El aporte energético para la formación del ATP proviene de la energía libre del entorno, la que entonces queda recuperada como energía química en este enlace. La energía liberada al producirse la ruptura, se utiliza en los distintos tipos de trabajos celulares. Por lo tanto, podemos decir que el ATP cumple un ciclo como intermediario energético: la célula consume ATP para generar distintos trabajos, y genera simultáneamente ADP. Pero, al tomar del entorno la energía libre, ese ADP es fosforilado a ATP nuevamente, y comienza nuevamente el ciclo. 4.5.- Enzimas, las catalizadoras de los procesos metabólicos. 4.5.1.- Metabolismo celular. • Es el conjunto de reacciones bioquímicas que ocurren en el interior de una célula. • Son reacciones ordenadas, eficaces y específicas, debido a que cada una de ellas está catalizada por una enzima. • Se puede resumir en los siguientes procesos: o Obtención de E química a partir de moléculas orgánicas combustibles, o de la luz solar, en AMBOS casos provenientes del entorno (exógenos). o Conversión de los principios nutritivos exógenos en precursores de macromoléculas de la célula. o Ensamblaje de estos precursores en proteínas, ácidos nucleicos, lípidos, otros componentes celulares. o Formación y degradación de las bio-moléculas que cumplen funciones especializadas de la célula. • Su molécula impulsora de energía es el ATP. • Se divide en 2 fases: catabolismo, y anabolismo. Ambos, están diferenciados en el apartado “4.1.3.- Ciclo del ATP” 4.4.2.- Enzimas. • Son catalizadores biológicos que aumentan la velocidad de las reacciones químicas. • Las enzimas reducen la Energía de Activación, que es una energía para que se activen los reactivos. No afectan a la variación de energía libre (G) ni el Keq. • Son proteínas, las moléculas sobre las que actúan se llaman Sustratos y las que resultan de las reacciones, Productos. Tienen estructura 1º, 2º, y 3º globular. • Son altamente específicas, lo que significa que sólo participan en determinadas reacciones, uniéndose a determinados sustratos en los llamados Sitios Activos. • Son eficientes en pequeñas cantidades; son reutilizables, porque no se alteran durante la catálisis, y son reversibles las uniones enzima-sustrato. • Existen dos modelos de unión enzima-sustrato: o Modelo Llave-Cerradura: Establece la total complementariedad entre el sitio activo de la enzima y el sustrato sobre el cual actúa, como una llave con su cerradura. o Modelo de Encaje Inducido: la complementariedad entre el sitio activo y el sustrato se alcanza luego de la interacción entre ellos, ya que involucra una modificación en los sitios activos de algunas enzimas. Clasificación • Simples: la parte proteica posee actividad catalítica por sí sola. • Conjugadas: además de la parte proteica (apoenzima) requieren de otra sustancia no proteica (cofactores enzimáticos) para tener capacidad catalítica. Los cofactores enzimáticos pueden ser Iones inorgánicos o moléculas orgánicas pequeñas, pudiendo ser una coenzima (unión no covalente) o grupo prostético (unión covalente). Las enzimas activas (apoenzima unida a su cofactor) se las llama Holoenzimas. Cinética enzimática. Estudia la velocidad de las reacciones en presencia de enzimas. Los factores que la afectan son: • Temperatura: las reacciones enzimáticas tienen un T óptima a la cual se alcanza la mayor actividad, que luego disminuye ya sea que se aumente la temperatura o se disminuya. • pH: la actividad enzimática está modulada por el pH, siendo que hay un pH óptimo donde esta sea máxima, y que luego la actividad decaerá si es modificado. • [E]: manteniendo los demás factores constantes, la velocidad de reacción aumentará a medida que la concentración de sustrato también lo haga. • [S]: como el caso anterior, a mayor concentración de sustrato, mayor velocidad. Pero tiene una restricción este caso, ya que llegado a un cierto punto la enzima se satura (todos los sitios activos están ocupados y se alcanzó la velocidad máxima) y la velocidad permanece constante. El Km es la concentración de sustrato necesaria para alcanzar la mitad de la velocidad máxima. A menor Km, mayor afinidad del sustrato por la enzima, mayor saturación, y mayor velocidad. • Inhibidores: sustancias que disminuyen o suprimen completamente la actividad de una enzima. Pueden ser: o Inhibición reversible: disminuyen la actividad enzimática, ya que se unen reversiblemente a la enzima. Hay dos tipos: § Competitiva, donde el inhibidor tiene estructura similar al sustrato, y compiten entre ellos para ver quién se une a la enzima. Si se une enzima-inhibidor, reduce la [S], la velocidad de reacción disminuye (puede llegarse a la Vmáx si se aumenta demasiado la [S]) y el Km aumenta (pierde su afinidad). § No Competitiva, donde el inhibidor no competitivo puede unirse sin competir con el sustrato ya que se une en otro lado. En este caso, la enzima se inactiva y es incapaz de generar productos porque se producen cambios conformacionales en la misma, que son irreversibles aumentano la [S]. No se modifica el Km (ni su afinidad), pero la Vmáx disminuye. o Inhibición irreversible: producen un cambio permanente en la enzima cuando el inhibidor se une a ella, desembocando en la pérdida definitiva de su actividad. • Regulación de la actividad enzimática: puede ser por un mecanismo a largo plazo (lentos), ya que operan a nivel genético modificando la [E], y pueden ser Inducción (aumenta la síntesis de la enzima) o Represión (disminuye la síntesis de la enzima). O mecanismos a corto plazo (rápidos), ya que modifican la actividad enzimática sin modificar la [E]. Estos son: o Regulación alostérica: mediante enzimas alostéricas. § Poseen estructura cuaternaria y son proteínas oligoméricas. § Tienen un sitio activo donde se une el sustrato, y además, tienen uno o más sitios alostéricos donde se unen los moduladores alostéricos (moduladores positivos aumentan la afinidad enzima-sustrato, y los negativos la disminuyen). § Curvas sigmoideas de velocidad de reacción. Esto significa que a bajas [S] la V es baja, mientras que cuando la [S] aumenta, la V aumenta en forma marcada. § Catalizan reacciones irreversibles del metabolismo. § Generalmente están al comienzo de las vías metabólicas. § Feed-back o retroalimentación: alguno de los productos finales de la vía puede actuar como modulador alostérico negativo. § Activación por precursor: algún precursor de la vía metabólica puede actuar como modulador alostérico positivo. § Se saturan. o Regulación por modificación covalente: Se produce por fosforilación o desfosforilación (unión/eliminación de fosfatos) de algunas enzimas. Las enzimas que fosforilan (con gasto de ATP) son las Quinasas; las que desfosforilan son las Fosfatasas. ZIMÓGENOS: son enzimas que se sintetizan como precursores inactivos de otras. Se activan por pérdida de un péptido y si fueran todo el tiempo activas, probablemente, serían autodestructivas. Deben eliminarse las partes inactivas, para dejar libres a las activas y que el zimógeno tenga actividad. UNIDAD TEMÁTICA 2 ORGANIZACIÓN DEL CITOPLASMA CAPÍTULO 5: Estructura y función de la membrana plasmática. 5.1.- Organización molecular. Vista al microscopio electrónico, se reveló que la membrana está formada por una capa triple formada por dos capas externas oscuras delimitando una tercera clara y ubicada en el centro. La parte oscura corresponde a las cabezas polares de los fosfolípidos, y la parte media y clara serían las colas hidrofóbicas de los mismos. 5.2.- Composición química. • Lípidos: son, en su mayoría, fosfolípidos, aunque hay glucolípidos y colesterol. Constituyen la lámina continua que envuelve a la célula y la limita. Constituyen la barrera de permeabilidad. • Glúcidos: siempre combinados con proteínas o lípidos, siempre están unidos covalentemente de modo que queden dispuestos hacia el espacio extracelular. Suelen ser oligosacáridos compuestos por distintos monosacáridos. Tienen función de reconocimiento celular. • Proteínas: participan en la organización estructural, la permeabilidad, como receptores y transmisores de señales (enzimas).
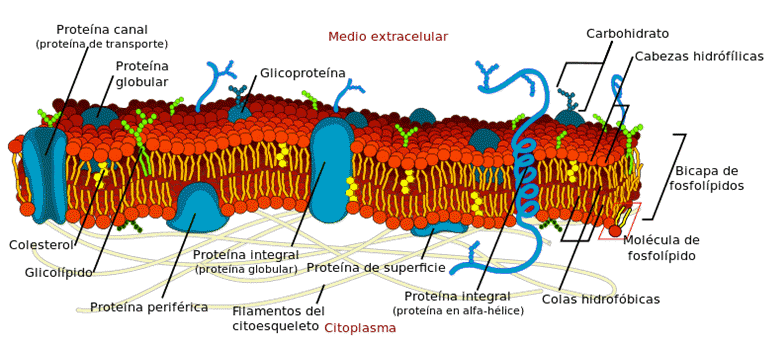
Pueden ser INTEGRALES ó PERISFÉRICAS. 5.2.1.- Disposición de Lípidos. La mayoría son fosfolípidos, que tienen una cabeza polar (afín con el agua) y los dos ácidos grasos (insolubles en agua), siendo así moléculas anfipáticas (por esto espontáneamente forman bicapas en medios acuosos). • En las membranas, los lípidos se organizan formando dos superficies hidrofílicas separadas por una zona central hidrofóbica, de modo tal que los grupos hidrofílicos estén expuestos al medio acuoso en el exterior celular y al agua del citoplasma. • La bicapa lipídica NO es estática, sino que las moléculas que la componen se mueven, formando una capa fluida. Los movimientos que realizan los fosfolípidos son: o Lateral: se mueven de lugar en la misma capa en la que están. ○ Rotación: giran sobre sí mismos. o Flexión: cambia como si fuera un espejo. o Flip-flop: un fosfolípido de una capa pasa a la otra. • La membrana es asimétrica, porque la distribución de lípidos entre una y otra monocapa, es distinta. • En las membranas de las células animales, también se encuentra el colesterol. Está molécula mantiene separadas parte de las cadenas de los ácidos grasos de los lípidos y reduce la movilidad de estos, haciendo menos fluida la membrana y menos permeable. • Además de fosfolípidos, hay esfingolípidos en las membranas biológicas. Estos están en mucha menos proporción que los anteriores, y se los suele encontrar mayormente en el tejido nervioso. Los gangliósidos y cerebrósidos están presente en la cara externa. 5.2.2.- Disposición de glúcidos. Son en general oligosacáridos lineales o ramificados, que están asociados a proteínas (glucoproteínas) o a lípidos (glucolípidos). • Siempre se los encuentra “mirando” al exterior celular, por tanto tienen también disposición asimétrica. • Participan en el reconocimiento celular. • Pueden aparecer también como Proteoglicanos. • Integran el glucocálix, una cubierta que protege a la delicada superficie celular. 5.2.3.- Disposición de proteínas. Siguen el modelo de mosaico fluido de las membranas. En este modelo se postula una bicapa lipídica continua, que está interrumpida en algunos sitios por proteínas que la atraviesan total o parcialmente (como un mosaico) y favoreciendo la asimetría de estas. A. Proteínas integrales o intrísecas. • Son aquellas que atraviesan la membrana. • Tienen partes hidrofóbicas (interactúan con los AG de los lípidos) y partes hidrofílicas (que miran al exterior celular, junto con las cabezas polares). • Pueden ser: o Estructurales: función mecánica, como por ej.: el anclaje del citoesqueleto. o Transportadoras o carriers: llevan sustancias de un lado a otro de la membrana. o Con función enzimática: son pequeñas “bombas” que extraen e introducen algún ion, con gasto de energía por parte de la célula, realizando un transporte activo, en contra del gradiente de concentración. o Polares: forman parte de los poros, constituyendo pequeños “canales” por los que pasan sustancias hidrofílicas cargadas (iones). o Receptoras y transductoras: de la señal de éstos canales (de iones, ya que no pueden hacerlo por la membrana), y/ó bombas (utilizan energía para bombear, dentro y fuera, iones). o Con propiedades antigénicas: son capaces de comportarse como antígenos, que marcan la superficie de la célula como una “etiqueta”, y permite que sea reconocida por otras células. B. Proteínas periféricas. Se unen a las regiones expuestas y polares de las proteínas integrales o a las cabezas polares de los fosfolípidos, por fuera de la bicapa, mediante enlaces electrostáticos débiles. Se encuentran dispersas y pueden ser extraídas fácilmente sin afectar a la bicapa lipídica (fosfolípidos). Algunas de las proteínas periféricas más conocidas, son la actina o la espectrina (ancladas al citoplasma/cara interna). 5.3.- Características y propiedades. • TODAS las células poseen membrana plasmática, que las contiene y limita. • Gracias a ella, la célula puede nutrirse, mantener sus componentes, creer, reproducirse, liberar desechos de su metabolismo, obtener materia y energía. • Posee una estructura compleja, responsable del control de funciones vitales para la célula. • Carece de resistencia mecánica, y en muchas células se encuentra reforzada por otras cubiertas más gruesas y complejas, como la pared celular de las células eucariotas vegetales. • Es como la “piel” de la célula: ya que es capaz de recibir estímulos y dar lugar a que la célula pueda responder a ellos, a través del reconocimiento de las etiquetas membranales: los “antígenos específicos”. • Es incapaz de evitar la desecación, ya que el agua puede atravesarla de diferentes maneras. • Tiene una permeabilidad selectiva: es capaz de regular el intercambio de materiales entre la célula y el medio quela rodea. Esto permite un transporte restrigido de agua y solutos (ST). • Mantiene la homeostasis: es la responsable de mantener la diferente composición química entre la célula y el medio extracelular, ya que ambos medios (intra y extra) están separados por la membrana. 5.4.- Funciones. • Protección. • Contención del protoplasma. • Control del medio interno: el medio intracelular debe ser estable porque allí tendrán lugar las reacciones bioquímicas y las transformaciones que sufre la energía para realizar las funciones vitales. Asimismo, algunas reacciones requieren de enzimas, y estas sólo actúan de manera correcta bajo ciertas condiciones. Está función se denomina homeostasis. • Intercambio de moléculas: la célula obtiene materia del medio extracelular, así como también vierte sustancias al medio intracelular (secreciones propias, desechos metabólicos). • Receptividad de señales extracelulares. • Reconocimiento celular. • Anclaje de moléculas del citoesqueleto o de la matriz extracelular. • Compartimentalización de dominios celulares: separa dos dominios de diferente composición y concentración química. • Adhesión y comunicación entre células. • Permeabilidad selectiva: la bicapa lipídica confiere a la membrana baja permeabilidad a las moléculas hidrofílicas y con carga, sólo permitiendo el paso de aquellas que cumplan con determinadas características fisicoquímicas y de tamaño. 5.5.- Transporte a través de la membrana.
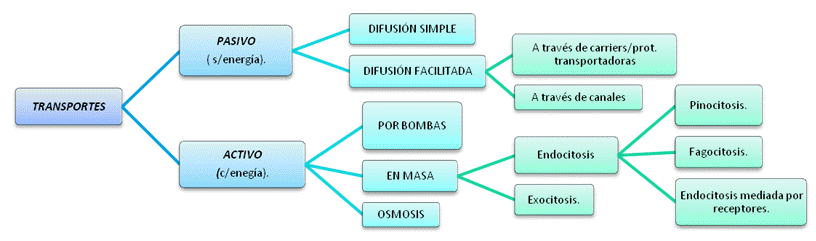 Si en el transporte (tanto TA como difusión facilitada) pasan 2 solutos (ST) en la misma dirección, se llama Simporte o Cotransporte. Si en cambio, transporta 2 solutos (ST) pero en direcciones contrarias, se llama Antiporte o Contratransporte. PERO, si sólo pasa UN soluto (ST) se llama Uniporte o Monotransporte, para cualquier dirección.
5.5.1.- Transporte pasivo.
• NO requiere del gasto de energía metabólica.
• Ocurre en sentido del gradiente de concentración del soluto en cuestión.
DIFUSIÓN: desplazamiento de moléculas de soluto (ST) desde una región de mayor concentración ([C]), a otra con menor [C], A FAVOR del gradiente de concentración, hasta llegar al equilibrio.
A. Difusión simple.
• Se produce directamente a través de la membrana, SIN resistencia.
• Puede ocurrir a través de la bicapa lipídica, o de los canales proteicos abiertos.
• Es un movimiento directo, que permite el paso de moléculas no polares o hidrofóbicas.
B. Difusión facilitada.
• Requiere de un trasportador o canal, para atravesar la membrana a favor del gradiente de concentración.
• Son las proteínas integrales de membrana quienes cumplen esta función (transportadores y canales).
Difusión facilitada por proteínas de transporte o carriers
Los transportadores forman una unión específica transportador-soluto, que cambia la conformación de la proteína para que libere al soluto (ST) en la superficie opuesta a la de entrada. Luego vuelven al estado inicial y se repite el proceso.
Si en el transporte (tanto TA como difusión facilitada) pasan 2 solutos (ST) en la misma dirección, se llama Simporte o Cotransporte. Si en cambio, transporta 2 solutos (ST) pero en direcciones contrarias, se llama Antiporte o Contratransporte. PERO, si sólo pasa UN soluto (ST) se llama Uniporte o Monotransporte, para cualquier dirección.
5.5.1.- Transporte pasivo.
• NO requiere del gasto de energía metabólica.
• Ocurre en sentido del gradiente de concentración del soluto en cuestión.
DIFUSIÓN: desplazamiento de moléculas de soluto (ST) desde una región de mayor concentración ([C]), a otra con menor [C], A FAVOR del gradiente de concentración, hasta llegar al equilibrio.
A. Difusión simple.
• Se produce directamente a través de la membrana, SIN resistencia.
• Puede ocurrir a través de la bicapa lipídica, o de los canales proteicos abiertos.
• Es un movimiento directo, que permite el paso de moléculas no polares o hidrofóbicas.
B. Difusión facilitada.
• Requiere de un trasportador o canal, para atravesar la membrana a favor del gradiente de concentración.
• Son las proteínas integrales de membrana quienes cumplen esta función (transportadores y canales).
Difusión facilitada por proteínas de transporte o carriers
Los transportadores forman una unión específica transportador-soluto, que cambia la conformación de la proteína para que libere al soluto (ST) en la superficie opuesta a la de entrada. Luego vuelven al estado inicial y se repite el proceso.
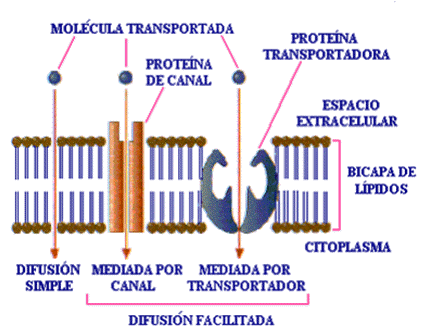
Estas proteínas transportan MOLÉCULAS y presentan cinética de saturación. Difusión facilitada por canales. Las partículas ingresan y egresan por canales. Éstos, son muy selectivos y pequeños, ya que SOLO permiten transportar IONES inorgánicos. La apertura y cierre de éstos, se regula por 3 mecanismos distintos: • Por voltaje: se abren o cierran cuando cambia el potencial eléctrico a ambos lados de la membran. • Por ligamiento (señales químicas): necesitan de ciertas sustancias que llegan desde el exterior y se unen al “receptor-canal”, modificando su apertura. • Por volataje y ligado: es un tipo particular de receptor/canal, que requiere tanto de cambios en el voltaje, como de la unión de una sustancia desde el ext. De la célula. Además de usar el gradiente de concentración, utilizan el gradiente electroquímico. 5.5.2.- Trasporte activo. • Transporta moléculas de una zona con menor [C], hacia otra de mayor [C]. • Va en contra del gradiente de concentración. • NECESITA energía. A. Transporte activo por bomba. Está mediado por una proteína integral de membrana, llamada “bomba” (hace de canal y enzima al mismo tiempo). El modelo más estudiado es el de la bomba de Na+/K+, que saca Na+ de la célula e ingresa K+ a ella. Este trabajo lo hace hidrolizando al ATP (ATPasa), rompiendo el enlace entre el 2º y 3º Pi, de modo que saque 3 Na+ e ingrese 2 K+. B. Transporte activo en masa.
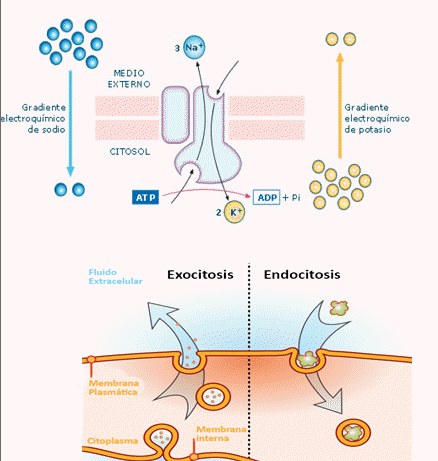
Las partículas entran o salen de la célula en masa, “arrastrando” una porción de la membrana (forma vesículas con ese pedazo). Se divide en dos: • EXOCITOSIS: consiste en un proceso por el cual se libera material intracelular (mediante vesículas) al espacio extracelular. Las vesículas transportadoras se dirigen desde el medio intracelular hacia la zona de la membrana plasmática, donde recibirán señales específicas del medio. Allí, una serie de cambios, llevan a la fisión y fusión posterior de las vesículas con la membrana plasmática, y el contenido intracelular transportado, saldrá al espacio extracelular. • ENDOCITOSIS: por este transporte, ingresan sustancia del medio extracelular al intracelular. Se lo considera como el proceso de digestión INTRA-celular, el cual esta mediado por vesículas de transporte. Según el tamaño de éstas últimas, se la puede clasificar en 3 tipos: o Pinocitosis: transporta sustancias disueltas o porciones de líquido extracelular; y sus vesículas son pequeñas. o Fagocitosis: partículas son de mayor tamaño y en suspensión; sus vesículas son mayores que la pinocitosis. El proceso comienza con un estímulo a la membrana celular, donde algunas proteínas integrales actúan como receptores y reconocen una molécula del medio. Al hacerlo, se desencadena el proceso, fagocitándose la partícula y formando el fagosoma, utilizandose una porción de la membrana plasmática. o Endocitosis mediada por receptores: absorción de LDL. La lipoproteína de baja densidad (LDL) contiene mucho colesterol, rodeado por una bicapa lipídica con proteínas de gran tamaño. En la superficie celular, hay receptores específicos para la LDL, que se unen a ella y forman las fositas de la endocitosis. Estas fositas están revestidas por clatrina (proteína fibrosa). Mediante ciertas señales, se termina de cerrar la vesícula y se reciclan la clatrina, los receptores y la membrana de la vesícula (que vuelven a la superficie). Los lisosomas liberarán el colesterol de la vacuola que contiene la LDL.
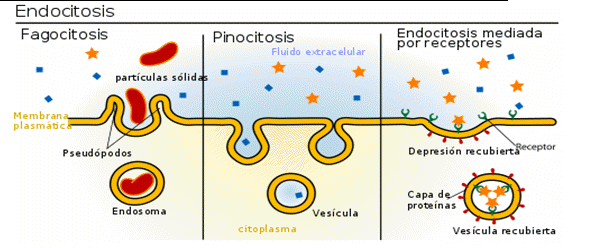
C. Ósmosis. Es la difusión del H2O desde la solución menos concentrada (hipotónica) hacia la solución más concentrada (hipertónica) para lograr el equilibrio (solución isotónica). Las soluciones están en dos compartimientos separados por una membrana semipermeable (permeable al H2O pero no al soluto). El H2O dejará de difundir cuando la presión de su columna se lo impida (Presión osmótica), y se haya llegado al equilibrio. CAPÍTULO 6: Sistema de endo-membranas y los perorixomas. 6.1.- Sistema vacuolar citoplasmático (SVC). • SÓLO en célula EUCARIOTAS. • Es un sistema tridimensional de tubos, cisternas (bolas aplanadas), y vesículas, conectados entre sí y formados por endomembranas. • Las organelas que lo integran son: Envoltura nuclear, REG, REL, Complejo de Golgi, Endosomas y Lisosomas. Funciones: • Compartimentalización del citoplasma (lo divide en 2: por un lado está la matriz citoplasmática/citoplasma/citosol, y por otro, los compartimientos con endomembrana) y de sistemas enzimáticos. • Realiza intercambios con el citosol por permeabilidad selectiva de sus endomembranas. • Proporciona vías de conducción intracelular para sustancias. • Contribuye al sostén y mantenimiento de la estructura celular. Origen Se lo considera como la evolución de la membrana plasmática procariota. La cara interna de las membranas del SVC son semejantes a la cara externa de la membrana plasmática de las células procariotas. Por ello, se supone que estas endomembranas se originaron por una invaginación y separación de la membrana plasmática procarionte, formando vesículas intracelulares. Mecanismo de transporte: gemación, y fusión de vesículas. Las dependencias del SVC se comunican indirectamente, a través de vesículas membranosas que se desprenden de ellas (por gemación) y se funcionan con otras. De esta manera, se transfieren de un lado a otro, fragmentos de membranas y sustancias contenidas en el interior de dichas vesículas. 6.1.1.-Rentículo Endoplasmático (RE). A. Rentículo Endoplasmático Rugoso (REG). • Está conectado a la envoltura nuclear. • Está formado por sistemas de cisternas ordenadas y paralelas entre sí, formando pilas de membranas que se comunican por delgados túbulos membranos. • Tiene ribosomas adorsados a su cara externa. Procesos biosintéticos del REG, asociados a la membrana. El REG se encarga de realizar la síntesis, plegamiento y glicosilación parcial de proteínas; como así también degradación y expulsión de aquellas mal plegadas. Las proteínas resultantes son las de todas las membranas (biosíntesis de membranas); las proteínas de exportación; del interior (luz) del SVC; y las enzimas hidrolíticas (lisosomas). Ribosomas del REG. • Compuestos por ARNr + proteínas. • Pueden encontrarse en la célula, ya sea libres, o unidos por una molécula de ARNm (polisomas), o bien, adheridos a las membranas del REG. • Son fundamentales para la síntesis de proteínas: TODAS las proteínas comienzan su síntesis en los ribosomas libres, pero según cuál sea el destino de éstas, los mecanismos serán distintos. Distribución intracelular de proteínas desde el REG y sus ribosomas. • Si las proteínas deben finalizar su síntesis en el REG (y son propias de éste), éstas tendrán una péptido señal en el extremo NH2terminal. La péptido señal asomará por el ribosoma y será reconocida por las partículas SRP (proteína de reconocimiento de la señal) del citosol. Las 2, en conjunto (señal + SRP), son reconocidas por un receptor de la membrana del REG (proteína integral), y entonces la proteína ingresará a la luz de la cisterna del REG. Una vez dentro, la enzima peptidasa señal elimina el péptido señal de la proteína, y esta queda completa. • Si las proteínas deben finalizar su síntesis en el REG, PERO su destino final es la membrana plasmática, éstas tendrán solo una señal de anclaje que será reconocida por la membrana de cada organela. • Si las proteínas se sintetizan por completo en los ribosomas libres (es decir que, no solo empiezan su síntesis allí, como cualquier tipo de proteína, sino que también la finalizan en el mismo lugar), éstas PUEDEN ó NO tener señal. Las que NO TIENEN señal, son las que permanecen en el citosol(ej. enzimas de la glucólisis). Las que SÍ TIENEN SEÑAL, son las que están destinadas a organelas específicas (mitocondria, núcleo, etc.), y éstas marcan entonces su destino de finalización. B. Rentículo Endoplasmático Liso (REA - REL), • Conjunto de túbulos y vesículas, más desordenados que el REG, que se comunican entre sí por vesículas. • No posee ribosomas. • Su disposición es irregular. • Función: Síntesis de lípidos; Glucogenolisis (degradación de glucógeno), Almacenamiento de Ca++, Detoxificación de drogas, alcohol y fármacos (citocromo p450); Producción de enzimas para la síntesis de colesterol. 6.1.2.- Complejo de Golgi. • Está formado por bolsas aplanadas (cisternas) concéntricas. Presenta una cara cóncava y otra convexa. La primera, es la cara de maduración o “trans”, libera vesículas de secreción con los productos modificados. La segunda es de formación o “cis”, recibe productos del REG y del REL. • En células vegetales sus cisternas apiladas y dispersas, se las llama dictiosomas. • Funciones: o Distribuye y direcciona los productos del REG, a diferentes organelas, membrana y exterior celular. o Ocupa “el centro” del tráfico vesicular. o Sintetiza glúcidos (glucosaminoglucanos y oligosacáridos) y proteoglicanos. o Glicosila proteína y lípidos que recibe del REG y del REL respectivamente, transformándolos en glicoproteínas y glicolípidos (enzimas: glicosil-transferasas). o Concentra y empaqueta proteínas de exportación y enzimas hidrolíticas (lisosomas). o Marca a las enzimas lisosomales, uniéndoles Manosa-P. o Produce los lisosomas. o Participa en la secreción celular. 6.1.3.- Lisosomas. • Son pequeñas vesículas membranosas que sobresalen del Golgi. • En ellas se produce el desdoblamiento de moléculas orgánicas complejas, gracias a las enzimas hidrolíticas que contienen (hidrolasacácidas). • Constituye el “sistema digestivo celular”, gracias a la permeabilidad selectiva de su membrana glicosilada (autoprotección). • Tienen pH=5, mantenido por su propia bomba de H+. • Se clasifican en primarios y secundarios. Los primarios solo contienen enzimas hidrolíticas, sintetizadas en el REG y procesadas luego en el Golgi. Los secundarios en cambio, contienen partículas digeridas por las hidrolasas. Pueden ser partículas extrañas (heterofagocitosis) o propias de la célula (autofagocitosis). 6.1.4.- Endosomas. • Conjunto de vesículas y túbulos, distribuidos en la periferia celular. • Se clasifican en endosomas tempranos, y tardios. Los primeros, llamados también proces, son los recién formados y están cerca de la membrana. Los tardios en cambio, ya han viajado bastante, y se encuentran alejados de la membrana, cerca del Golgi. • Su diferencia con los lisosomas, es su gran contenido de enzimas y su menor grado de acidez. Tienen pH=6, el cual también está regulado por una bomba propia de H+. • Funciones: transporte de moléculas endocitadas, y reciclado de ciertas moléculas (Ej. Clatrina, receptores). 6.2.- Ciclo secretor. Involucra solo al complejo de Golgi y sus lisosomas, y a los RE. 1. El complejo de Golgi recibe en su cara convexa a las proteínas, lípidos y lipoproteínas de los RE. 2. Una vez en el interior de las cisternas del Golgi, el material es modificado por agregar o eliminar partes de las moléculas, y condensado por extracción de líquido, mientras va circulando hacia la cara trans. 3. Cuando llegan a la zona de maduración (trans), el material es empaquetado con una membrana apropiada, formándose así la vacuola condensante, que sigue perdiendo agua a medida que viaja hacia la membrana plasmática. 4. Luego de la condensación, se forma el gránulo de secreción, donde se almacena el producto. Éste llega hasta la membrana plasmática, y su membrana se fusiona con ella para liberar su contenido por exocitosis. 5. El aumento de la superficie membranosa causado por la exocitosis, es compensado por endocitosis. De lo expuesto, se entiende que debe haber un flujo permanente de membranas que vayan reponiendo la región del Golgi que se pierde por la cara de maduración. 6.3.- Digestión intracelular: endocitosis mediada por vesículas de transporte. Como explicamos en el capítulo anterior (n°5), la membrana tiene varios mecanismos de transporte; sin embargo, sólo UNO de ellos conforman a la digestión intracelular: la ENDOCITOSIS, ya que se trata de un proceso de degradación de sustancias DENTRO DE LA CÉLULA (medio intracelular). Éste, está mediado por vesículas de transporte, que cumplen funciones específicas dentro del medio. La EXOCITOSIS NO forma parte de éste proceso, porque conformaría la digestión EXTRA-celular, ya que libera partículas fuera del medio interno. Vesículas de transporte: formación, traslación y destino. Las vesículas transportadoras son simplemente TIPOS de lisosomas secundarios. Estas vesículas de transporte, se clasifican en vacuolas digestivas o heterofagosomas, y en vacuolas autofágicas ó citolisosomas, según su función dentro de la digestión. Las primeras, se encargan de atacar al material incorporado al medio intracelular, para degradarlo y convertirlo en moléculas sencillas. Las segundas en cambio, realizan el proceso contrario: facilitan la renovación de dicho material atacado anteriormente. Proceso de digestión intracelular. La digestión comienza cuando los materiales volcados en los endosomas precoces, son descargados en los tardíos. Aquí, comienzan a fusionarse las membranas de dichos endosomas, con las de las vesículas lisosomales, y se forman los lisosomas secundarios. Los lisosomas secundarios contienen una gran cantidad y variedad de enzimas hidrolíticas que van a atacar al material incorporado, degradándolo a partículas simples; o sea, se encargan de descomprimir/desdoblar macromoléculas, y convertirlas en moléculas más sencillas (ó monómeros). Estos lisosomas, reciben el nombre de vesículas digestivas, por su poder reduccional: • Las proteínas se desdoblan por acción de la peptidasa, • Los ácidos nucleicos se simplifican por acción de nucleasas. • Los hidratos de carbono se descomprimen por acción de las amilasas. Finalmente, las moléculas simples como monosacáridos, aminoácidos, y nucleótidos, resultantes de la digestión, pueden tomar 2 caminos: • La 1ª opción, sería pasar al citoplasma a través de la membrana del lisosoma secundario o vacuola digestiva, gracias a ciertas proteínas transportadoras especiales. • La 2ª opción, sería formar autofagosomas ó vacuolas autofágicas. Éstos, son otro tipo de lisosomas secundarios, que pueden llegar a destruir a la célula. Su función, sería englobar organelas intracelulares, como mitocondrias o partes del sistema vacuolar, en un proceso de autofagia, que posibilita la renovación de las estructuras degradas por las vesículas digestivas, o sea, unir de nuevo a las moléculas simples para formar macromoléculas. 6.4.- Perorixomas. NO FORMAN PARTE DEL SVC. • Son vesículas pequeñas formadas por una membrana, en la que contienen enzimas oxidativas. • Sus enzimas están involucradas en el metabolismo del agua oxigenada/peróxido de hidrógeno (H2O2). Éste es un oxidante tóxico para la célula, que a su vez, degrada naturalmente ciertas moléculas orgánicas. • Tipos de enzimas: o Peroxidasas: capaces de utilizar el oxígeno molecular como medio para captar hidrógeno, y formar agua oxigenada. o Catalasa: enzima oxidativa. Se encarga de destruir al peróxido de hidrógeno (acción opuesta a la peroxidasa), o bien, de utilizarlo para oxidar alcoholes y sustancias tóxicas como drogas. También, se encarga de eliminar las moléculas de peróxido acumuladas. o Urato-oxidasa: enzima oxidativa que está muy concentrada, formando casi un cristal. • En las células vegetales, se encargan de degradar los ácidos grasos por beta-oxidación, como las mitocondrias en células animales. CAPÍTULO 9: Mitocondrias y Respiración aeróbica.
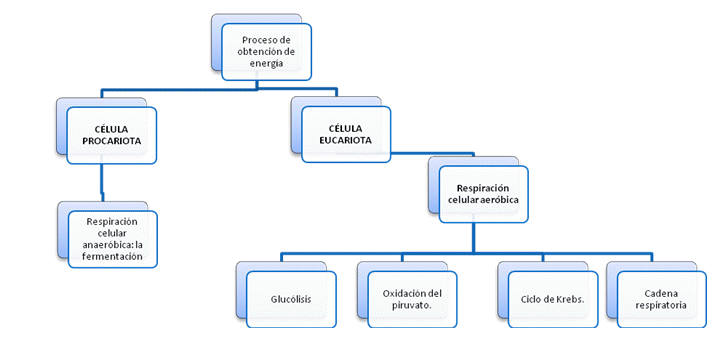
9.1.- Mitocondrias. Son organelas presentes en el citosol de las células eucariotes autótrofas y heterótrofas. Su forma es variable, y depende tanto del tipo celular como de su estadio funcional. Por lo general, se pueden encontrar mitocondrias en aquellas regiones donde la demanda de energía es muy elevada. De hecho, son el lugar donde ocurre la respiración celular, procesos por el cual una célula obtiene ATP. También, intervienen en la oxidación de moléculas orgánicas. Junto con los cloroplastos, son las únicas organelas capaces de generar descendientes y de fabricar sus propias proteínas, por contener ADN desnudo y ribosomas propios. Sin embargo, su composición no es lo suficientemente resistente al medio externo, como para coexistir por sí sola. Es por ello que tienen una relación de mutualismo permanente con el resto de los componentes de la misma célula donde se encuentran. 9.1.1.- Estructura Tienen forma alargada o esférica, y su longitud es variable. Poseen dos membranas que difieren en su composición química y propiedades: la membrana externa, y la membrana interna: • La membrana externa es completamente lisa y permeable a moléculas pequeñas de hasta 6.000 dalton. Posee mayor cantidad de lípidos, colesterol y fosfatidilnositol, que la membrana interna; pero tiene menos cantidad de cardiolipinas. Los lípidos de las mitocondrias, se sintetizan en el REL. •
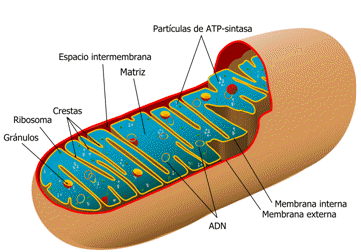
La membrana interna en cambio, tiene mayor proporción de proteínas que de lípidos. Es muy poco permeable a iones y protones. En ella se encuentran las proteínas que atraviesan la membrana y son transportadores específicos para ciertas sustancias como ATP, fosfatos, isocitrato, ácido pirúvico, y aminoácidos. También contiene sistemas de transporte para Ca++ y Mn++, y algunas proteínas aceptoras y transportadoras de electrones. Asimismo, en su cara interna, contienen al ATP sintetasa: complejo proteico asociado a la síntesis de ATP. Hacia adentro de la membrana interna, encontramos a las crestas. Éstas son pequeños pliegues de la propia membrana interna, que se proyectan hacia el interior de la organela (matriz mitocondrial). Su función es contener a las proteínas enzimáticas, nucleótidos, e iones. Entre ambas membranas, queda un espacio definido, llamado espacio de intermembrana, y al centro donde se extienden las crestas, se lo llama matriz mitocondrial. La matriz mitocondrial es una cámara continua, formada por un gel denso con alta concentración de proteínas solubles que participan en el proceso de respiración celular y en la oxidación de ácidos grasos. Allí también están los ribosomas del tipo procarionte y ADN circular, propios de la mitocondria, los cuales ya fueron nombrados anteriormente. 9.2.- La respiración celular aeróbica. ¡OCURRE SÓLO EN CÉLULAS EUCARIOTAS POR LA PRESENCIA DE OXÍGENO! En los organismos eucariotas, la respiración celular consiste en la combustión de macromoléculas para la obtención de energía. Estas macromoléculas, suelen ser (casi siempre) los monosacáridos, como la glucosa. Sin embargo, en ausencia de éstA, se puede acudir a los ácidos grasos (que generan más energía que la glucosa, pero también necesitan mucho más O2), o bien, a los aminoácidos (que funcionarán como último recurso de fuente inmediata, cuando haya ausencia de glucosa y de A.G). GLUCOSA (C6 H12 O6) + 6 O2 à 6 CO2 + 6 H20 + ENERGÍA (ATP) Por lo tanto, se puede caracterizar a La respiración celular como un proceso: • CATABÓLICO: porque se degrada una macromolécula (glucosa), para obtener moléculas sencillas e inorgánicas (como dióxido de carbono y agua). • EXERGÓNICO: porque la energía química obtenida por la ruptura de los enlaces químicos de los átomos de glucosa, es liberada al medio, y utilizada de 2 partes. A una se la transforma en energía calórica, y a la otra se la utiliza para formar ATP. • OXIDO-REDUCTIVO: porque con la oxidación de glucosa, se liberan átomos H+ (hidrógeno) y e- (electrones) que serán absorbidos por el oxígeno (O2) disponible en la célula, y se formarán moléculas de agua (H20). Vale aclarar que éste oxígeno, no es el que proviene de la oxidación de glucosa. El de la glucosa se utiliza para generar dióxido de carbono, y el oxígeno disponible en la célula, es el que se utiliza para generar agua. 9.2.1.- Etapas. 1. Glucólisis GLUCOSA + 2 ATP + 4 ADP + 2 Pi + 2 NAD+à 2 Ácido pirúvico + 2 ADP + 4 ATP + 2 NADH + 2 H+ + 2 H2O Es la “ruptura del azúcar”. Es un proceso catabólico y exergónico que ocurre en el citosol (citoplasma), y tiene como objetivo generar ácido pirúvico (piruvato). Cada reacción de la glucólisis es catalizada por su propia enzima: la fosfofructocinasa (FFK), enzima alostérica cuyos moduladores negativos son el ATP y el H+. Ésta es capaz de acelerar o frenar la glucólisis en respuesta a las necesidades energéticas de la célula. La glucolisis consiste de dos etapas: una que requiere energía (paso 1 y 2), y otra que libera más energía que la requerida anteriormente (paso 3). 1°: Se oxida la molécula de glucosa (de 6 carbonos//6C), y a su vez se le suman 2 grupos fosfatos (P) provenientes de 2 moléculas de ATP (que ahora quedan como ADP). El resultado será una molécula de azúcar fosfatada completamente inestable (fructosa-1,6-bifosfato).
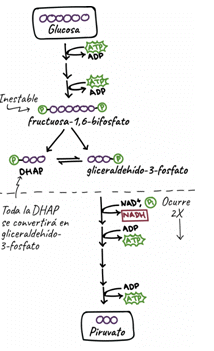
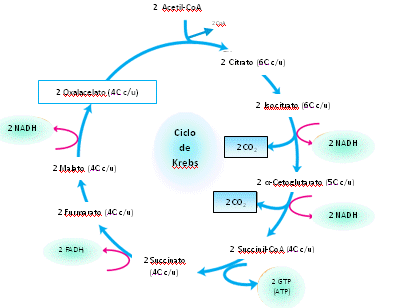
2°: Rápidamente, esta molécula de 6C, se divide en 2 moléculas de 3C y 1 P c/u (porque tenía los 6C de la glucosa, y además, los 2P de la oxidación). Éstas 2 moléculas se llaman: DHAP y P-GAL (gliceraldehido-3-fosfato). 3°: DHAP y P-GAL son oxidadas, y liberarán e-, átomos H+, y los 2 grupos P (un P por c/u). Entonces: el NAD+ se reduce al consumir los e- y los H+ liberados en la oxidación, y forma 1 molécula de NADH + H+. Los 2 P liberados oxidan a los 2 ADP que sobraron del paso 1, y forman 2 ATP y 1 molécula de agua (por lo que se recupera la energía perdida en el paso 1). Y con la finalización de la oxidación de DHAP y P-GAL, se forma 1 molécula de Piruvato o Ácido Pirúvico (de 3C). Sin embargo, recordemos que para que suceda el paso 1, se consumieron 2 ATP, y se los recupera en el paso 3. PERO como la glucolisis es exergónica (libera energía), no sólo debemos recuperar el ATP, sino que debemos fabricar el doble, para que éstos sean liberados y se cumpla la característica nombrada. POR LO TANTO, EL PASO 3 OCURRE DOS VECES: en una 1ª vuelta se recuperan los ATP, y en una 2ª vuelta se forma el ATP que se liberará al medio. ENTONCES: en vez de 1 molécula de NADH + H+, 2 ATP, 1 molécula de Piruvato, y 1 molécula de agua; SE FORMARÁN 2 MOLÉCULAS DE NADH + H+, 4ATP, 2 MOLÉCULAS DE PIRUVATO, y 2 MOLÉCULAS DE AGUA. EN RESUMEN... A partir de 1 molécula de glucosa de 6C, 2 ATP, y 2 P (provenientes de dicho ATP), se obtienen 2 moléculas de ácido pirúvico (piruvato) de 3C c/u, 4 ATP, 2 NADH + H+, y 2 moléculas de H2O. 2. Oxidación del ácido pirúvico/piruvato. Es la “descaboxilación oxidativa” del ácido pirúvico, PREVIO al ciclo de Krebs. Como ya vimos, el piruvato se produce durante la glucólisis en el citoplasma. Sin embargo, la oxidación del piruvato ocurre en la matriz mitocondrial, por lo tanto, las 2 moléculas de ácido pirúvico deberán atravesar la membrana mitocondrial para llegar a la matriz. Para ello, se acude a dos proteínas integrales: la porina y la translocasa, las cuales realizan un mecanismo simporte. Una vez dentro, comienza la modificación química de las 2 moléculas de piruvato. Aquí, interviene una enzima específica y varias coenzimas, entre ellas, la coenzima A (CoA). 1°: Se cortan los grupos carboxilos de cada piruvato, y se los libera en forma de 2 moléculas de CO2 (dióxido de carbono). El resultado serán dos moléculas de 2C c/u. 2°: Las 2 moléculas de 2C del paso 1, se oxidan y liberan electrones, transformándose en 2 grupos acetilos. Éstos son captados por 2 moléculas de NAD+, y se forman 2 moléculas de NADH + H+. 3°: Finalmente, los 2 grupos acetilos se unen a la coenzima A, y se forman 2 moléculas de Acetil-CoA que dan inicio al cilco de Krebs. ENTONCES... A partir de 2 moléculas de Piruvato y de 2 NAD+, se obtienen 2 moléculas de CO2, 2 moléculas de Acetil-CoA, y 2 moléculas de NADH + H+. 3. Ciclo de Krebs. Es una vía metabólica que ocurre dentro de la matriz mitocondrial. Consiste en una serie de 8 reacciones químicas, catalizadas por enzimas específicas. Por cada vuelta del ciclo, se oxida UNA molécula de Acetil-CoA. Como las moléculas de Acetil-CoA son DOS (provienen del paso anterior), y cada una tiene 3C, el ciclo debe dar 2 vueltas completas para que se oxide una molécula completa de glucosa, ya que ésta tiene 6C. Por lo tanto, CADA DOS VUELTAS AL CICLO, se oxidan 2 moléculas de Acetil-CoA ó 1 molécula de glucosa, y se transforman en 6 moléculas de CO2 (3 moléculas por c/vuelta). Mientras tanto, sus electrones y sus H+, formarán 10 moléculas de NADH + H+ y 2 moléculas de FADH2 (o bien, 5 NADH + H y 1 FADH2 por vuelta). Ac. Oxalacético + Acetil-CoA + GDP + Pi + 3 NAD+ + FAD à Ac. Oxalacético + CoA + 3CO2 + GTP + 3 NADH + 3 H+ + FADH2 + H2O El dióxido de carbono formado, sale de la matriz mitocondrial al citosol, y luego al exterior celular, atravesando las membranas por difusión simple. De allí, va a los capilares sanguíneos y es transportado por los glóbulos rojos Reacciones del ciclo de de Krebs. 1°: El acetil-CoA se une con una molécula de 4C (el oxalacetato) y libera su grupo CoA, a la vez que forma una molécula de 6C llamada citrato. 2°: El citrato se convierte en iso-citrato, y continúa con 6C. 3°: El isocitrato se oxida, y con el átomo de C liberado se genera una molécula de CO2. La nueva molécula de 5C se llama α-cetoglutarato. Durante este paso el NAD+ se reduce en NADH + H+. 4°: Es similar al tercero. En este caso, es la molécula de 5C la que se oxida. Al mismo tiempo, se vuelve a reducir otra molécula de NAD+ en NADH + H+, y se vuelve a liberar una molécula de CO2 a costa de la oxidación (ya que se perdió otro átomo C). La molécula de 4C resultante, se une a la coenzima A (que otorga el “CoA”) y forma un compuesto inestable (Succinil CoA). 5°: El complejo CoA se sustituye por un P, que luego se le otorga al GDP para obtener GTP. La molécula de 4C modificada en este paso se llama “succinato”. 6°: Se oxida el succinato y se forma otra molécula de 4C: “Fumarato”. En esta reacción se transfieren 2 átomos de H+ (junto con sus electrones) al FAD, para formar FADH2. 7°: Se le añade agua a la molécula de 4C (fumarato), y ésta se convierte en otra molécula de 4C, el “Malato”. 8°: Se regenera nuevamente el oxalacetato (el compuesto inicial de 4C) mediante la oxidación del Malato. En el proceso, otra molécula NAD+ se reduce en NADH + H+. EN RESUMEN... Cada 2 vueltas al ciclo, se utilizan 2 moléculas de Acetil-CoA (o sea 1 molécula de glucosa), de las cuales se utilizarán sólo 4 átomos de C (2 por c/Acetil-CoA), para formar 4 moléculas de CO2, 6 moléculas de NADH, 2 de FADH2, y 2 de GTP. 4. Cadena respiratoria y fosforilación oxidativa. Ambos procesos ocurren en la membrana interna de las crestas mitocondriales, entre la matriz mitocondrial y el espacio de intermembrana. • Fosforilación oxidativa: las moléculas de NADH y de FADH2 se oxidan en NAD+ + H+ y FAD + 2H+ respectivamente, para volver a ser utilizados por las primeras etapas de la respiración celular. De dicha oxidación, surge un gradiente de concentración de átomos H+, y una cadena de electrones constante, que serán utilizados en la cadena respiratoria. •
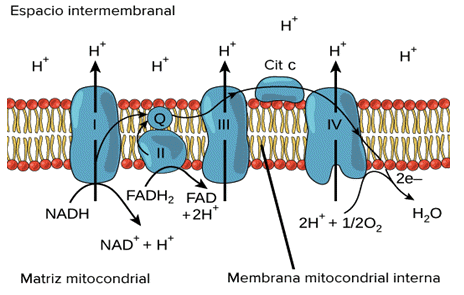
Cadena respiratoria: está formada por 6 aceptores secuenciales de electrones, los cuales se encuentran en la bicapa lipídica de las crestas mitocondriales. Éstos, son proteínas o complejos proteícos, conocidos como: Complejo I, Ubiquinona (simbolizado como “Q”), Complejo II, Citocromo C (simbolizado como “Cit c), Complejo III, y Complejo IV. A medida que la cadena de electrones (surgidos en la fosforilación oxidativa) pasa por los 6 aceptores, éstos van perdiendo la energía que contenían inicialmente. Al llegar al complejo III ó IV, éstos ceden los electrones que circulaban anteriormente al O2 (ultimo aceptor de electrones). Finalmente, el oxígeno con electrones se reduce, para combinarse con los átomos de H+ (surgidos del gradiente de concentración de átomos de H+), y se forman moléculas de agua. El resto de los átomos H+ que sobran del gradiente, son liberados al espacio intrermembrenal a través de los complejos I, III, y IV. Asimismo, la energía liberada por el transporte de e-, se utiliza para sintetizar más tarde ATP a partir de ADP + P. Por lo tanto, en esta última fase, ninguna de los dos pasos genera moléculas de ATP, sino que sólo generan un reacondicionamiento de aquellas moléculas “sobrantes” de las primeras 3 etapas, para que las mismas puedan volver a ser utilizadas por los primeros 3 pasos de la respiración celular. 9.2.2.- Balance energético. Recordemos quela respiración aeróbica, tiene como principal objetivo obtener energía a partir de la oxidación de glucosa. Esta energía, se la simboliza como moléculas de ATP, y para saber cuánta energía se produce por cada respiración realizada, debemos tener en cuenta las siguientes equivalencias que nos llevan al balance energético final: • 1 molécula de ATP/GTP = 1 molécula de energía (ATP). • 1 molécula de NADH + H+ = 3 moléculas de energía (ATP) • 1 molécula de FADH2 = 2 moléculas de energía (ATP) Entonces... 1. GLUCOLISIS: 2 ATP + 2 NADH + H+ (6 ATP) = 8 ATP. Por c/molécula de NADH + H+ se forman 3 moléculas de ATP. Como las moléc. de NADH + H+ obtenidas son 2, las moléculas de ATP obtenidas serán 6 (3 por cada molécula de NADH + H+). 2. OXIDACIÓN DEL PIRUVATO: 2 NADH + H+ = 6 ATP Ocurre lo mismo que en la glucolisis. 3. CICLO DE KREBS: 2 GTP ( = 2 ATP) + 6 NADH + H+ (= 18 ATP) + 2 FADH2 (4 ATP) = 24 ATP También pasa lo mismo que en los pasos anteriores, respecto al NADH + H+. Con respecto al GTP: es lo mismo que ATP, y en referencia al FADH2, por cada molécula de éste, se obtienen 2 moléculas de ATP. Como las moléculas de FADH2 obtenidas son 2, las moléculas de ATP resultantes serán 4 (2 por cada molécula de FADH2). ENTONCES, SE OBTIENEN EN TOTAL 38 moléc. de ATP ó de energía, considerando que la cadena respiratoria y la fosforilación oxidativa NO fabrian ATP. EN RESUMEN... ETAPA LUGAR PROPÓSITO MOLÉC. ENERGÉTICAS OBTENIDAS BALANCE ENERGÉTICO GLUCOLISIS Citoplasma Oxidar 1 moléc. De glucosa, para formar 2 de piruvato. 2 moléc. de ATP y 2 moléc. de NADH + H+. 8 ATP OXIDACIÓN DEL PIRUVATO Matriz mitocondrial Oxidar las 2 moléc. de piruvato, y transformarlo en 2 moléc. de Actil-CoA. 2 moléc. de NADH + H+ 6 ATP CICLO DE KREBS Matriz mitocondrial Reducir las 2 moléc. de Acetil-CoA, para generar 6 molec. de CO2. 2 moléc. de GTP, 6 moléc. de NADH + H+, y 2 moléc. de FADH2 24 ATP FOSFORILACIÓN OXIDATIVA Y CADENA RESPIRATORIA Crestas mitocondrial Reacondicionar las moléculas energéticas que quedaron dispersas, y generar también moléculas de agua. Ninguna. 0 ATP TOTAL DE ENERGÍA OBTENIDA 38 ATP. CAPÍTULO 10:

Cloroplastos y Fotosíntesis. 10.1.- Estructura de los cloroplastos. Estan presentes en el citoplasma de células autótrofas (vegetales y algunas algas). Es el lugar específico donde ocurre la fotosíntesis. Se caracterizan por tener color verde, debido a que éstos contienen a la clorofila: pigmento encargado de captar la energía lumínica del Sol. Cada planta contiene entre 20 y 40 cloroplastos, mientras que ciertas algas, solo uno. Es una organela de doble membrana, las cuales se encuentran delimitadas (separadas) por un espacio de intermembrana. La membrana externa es bastante permeable, y actúa como un “filtro” poco selectivo. La membrana interna en cambio, es más selectiva y posee proteínas de transporte especializadas en regularizar el pasaje de sustancias. Ésta, encierra un espacio a continuación de su cara interna, el cual da forma al estroma. El estroma es un gel fluido que ocupa un espacio delimitado de la membrana interna. En él se encuentran varias moléculas específicas, como las proteínas solubles que intervienen en la etapa bioquímica de la fotosíntesis. También, contiene tilacoides, y granas; y membranas tilacoidales (ó tilacoides del estroma)
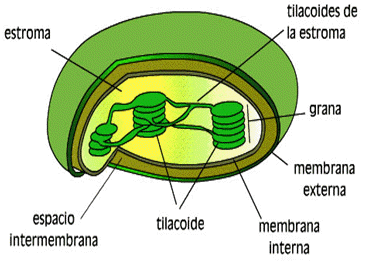
Los tilacoides son pequeños sacos aplanados (o “discos”) suspendidos dentro del estroma. Éstos, están conectados y superpuestos entre sí como si fuesen “pilas de monedas”, gracias al espacio intra-tilacoidal que los mantiene unidos (no se ve en el dibujo). La unión de varios tilacoides como “pilas de monedas” forman las granas. Las membranas tilacoidales ó tilacoides del estroma forman un tercer sistema de membranas, donde se pueden encontrar algunas enzimas y moléculas necesarias para la fotosíntesis (por ej.: la ATP sintetaza, los citocromos, y la plastoquinona). En su su bicapa lipídica se encuentra la clorofila, y otros pigmentos fotosintéticos contenidos en fotosistemas. (En el dibujo NO aparecen las membranas tilacoidales ni los fotosistemas) Los fotosistemas son complejos macromoleculares, que clasifican en 2 tipos. La diferencia entre un tipo u otro, radica en el TIPO de clorofila que contengan; en la LONGITUD de onda lumínica que puedan captar; en el PAPEL que juegan dentro de la fotosíntesis; y en la UBICACIÓN que tienen dentro de las membranas tilacoidales. FOTOSISTEMA DE TIPO 1, Ó “FS 1” FOTOSISTEMA DE TIPO 2, Ó “FS 2” TIPO de clorofila que contiene Clorofila unida a proteína Solo clorofila, junto con otros pigmentos sin unir. LONGITUD de onda que pueden captar 700 nm 680 nm FUNCIÓN dentro de la fotosíntesis Conforman el “centro antena” porque su función es capturar la energía lumínica y transferirla al “centro de reacción”. Conforman el “centro de reacción” porque se encargan de sintetizar los compuestos orgánicos. UBICACIÓN dentro de la membrana tilacoidal Cara externa de la membrana tilacoidal Cara interna de la membrana tilacoidal. Por otra parte, los cloroplastos (al igual que las mitocondrias) poseen su propio ADN, con el cual son capaces de fabricar sus descendientes, y sus propios ribosomas con el que sintetizan sus proteínas. Sin embargo, la falta de ciertas enzimas y de otras proteínas externas unidas a éstas (coenzimas), hace que NO puedan ser una estructura independiente, lo que genera una relación de mutualismo entre célula-cloroplasto. Además de los cloroplástidos, existen otros tipos de plásmidos importantes: • Los cromoplástidos son los que contienen aquellos pigmentos que dan color a las flores y los frutos: los carotenoides. Su origen proviene de la degradación de la clorofila en los cloroplastos, y pueden ser de color rojo, anaranjado o amarillo. • Los proplástidos y amiloplástidos son los que contienen gránulos de almidón, y funcionan como reservorios de energía. Se los puede encontrar en los tejidos vegetales de almacenamiento, vinculados principalmente con el crecimiento de las raíces y los tallos. 10.2.- Fotosíntesis. 6 CO2 + 6 H2O LUZ 6 C6H12O6 + 6 O2 Es el proceso por el cual los organismos autótrofos, sintetizan su propio alimento (compuestos orgánicos) a partir de moléculas inorgánicas y energía. Se considera que la fotosíntesis es: • ANABÓLICA: porque sintetiza macromoléculas (glucosa) a partir de moléculas sencillas e inorgánicas (dióxido de carbono y agua) • ENDERGÓNICA: porque absorbe energía lumínica para comenzar su proceso, y hasta se la transforma en energía química, para continuar aprovechándola. • OXIDO-REDUCTIVA: porque se oxidan moléculas de agua (pierden H+), y se oxida el dióxido de carbono (absorbe H+). La fotosíntesis ocurre en dos etapas: la primera es la fotoquímica, y la segunda es la bioquímica. ETAPA 1: FOTOQUÍMICA/FOTODEPENDIENTE/LUMÍNICA ETAPA 2: BIOQUÍMICA/FOTOINDEPENDIENTE/OSCURA LUGAR Membranas tilacoidales de las granas. Estroma. DEPENDE DE... La energía lumínica proveniente del Sol ATP y NADPH+ + H+ provenientes de la etapa fotoquímica. TIPO DE ENERGÍA Lumínica, porque depende del Sol. Química, porque no depende del Sol. MOLÉCULAS PARA INICIAR Agua (H2O), NADP+, y ADP + P Dióxido de carbono (CO2), ATP, y NADPH+ + H+ MOLÉCULAS OBTENIDAS (objetivo) ATP, NADPH+ + H+, y O2 ADP + P, NADPH+ y glucosa. 1. Etapa fotoquímica/fotodependiente/clara. En síntesis, la energía lumínica proveniente de la luz del Sol, es aprovechada para sintetizar ATP, a partir de ADP + P, y para reducir NADP+ en NADPH+ + H+. Los átomos de H+ que redujeron al NADP+, provienen de la oxidación del agua, cuyos átomos de O sobrantes, formarán oxígeno (o sea que, por c/molécula de agua (H2O), se liberan 2 átomos de H+ y 1 átomo de O, lo que formará 1 molécula de NADPH+ + H+, y ½ moléc. de Oxígeno). 1°: La energía lumínica ingresa al fotosistema I (el “C”), provocando que las moléculas de clorofila se exciten, y desprendan 2 electrones. 2°: Los 2 e- liberados, viajan hacia la molécula C (ferradoxina), y ésta los transporta hasta el NADP, para que se produzca (junto con los 2 átomos H+ de la oxidación del agua) su reducción: nos queda NADPH+ + H+. 3°: Como el fotosistema I perdió electrones, éste queda cargado positivamente y se produce un “hueco electrónico”, el cual será rellenado con los electrones que perderá el fotosistema II por acción (insinación) de la luz solar. Al quedar ahora el fotosistema II cargado positivamente, éste neutralizará su carga con los átomos de H+ provenientes de la oxidación del agua. Quienes transportan los electrones del fotosistema II al I son: la enzima A (plastoquinona), la enzima B (Plastocianina), y el complejo B (B6 - F) que funciona como intermediario entre las 2 enzimas (transporta los e- de la encima A a la B). Durante el pase de electrones, se liberará energía y se la utilizará para sintetizar ATP a partir de ADP +P en el estroma. ENTONCES... H2O + NADP+ + ADP + P LUZ NADPH+ + H+ + ATP + ½ O2 2. Etapa bioquímica/fotoindependiente/oscura. Es conocida como “el ciclo de Calvin-Benson”. Aquí, 6 moléculas de dióxido de carbono son reducidas por electrones y protones del NAPH+ + H+, y se ensamblan con la energía química del ATP, para formar glucosa. El dibujo que se observa a la derecha, refleja las proporciones de UNA vuelta al ciclo. Sin embargo, para que se obtenga una molécula de glucosa completa, el ciclo de Calvin debe repetirse 2 veces. Esto, se debe a que en UNA sola vuelta, entran 3 átomos de C con las 3 moléculas de CO2, y como la glucosa contiene 6C, en una sola vuelta se formaría ½ molécula de glucosa, no una completa. Por lo tanto, TODAS las proporciones representadas en el dibujo, se deben multiplicar x2, y así se obtendrá 1 molécula de glucosa neta con sus 6C correspondientes. 1°: Por acción de una enzima llamada rubisco, 6 moléculas de dióxido de carbono (CO2) se unen con 6 moléculas de Ribulosa difosfato (azúcar de 5C c/u presente en el estroma). 2°: De la unión anterior, se forman 2 compuestos inestables iguales de 6C, que rápidamente se divide en 12 moléculas de 3C c/u llamda “Ácido 3-fosfoglicérico” (3-PGA), o sea, 6 moléculas de 3-PGA por cada molécula inestable. 3°: Las 12 moléculas de 3-PGA son fosforiladas con 12 moléculas de ATP (1 ATP x cada 3-PGA), y luego se reducen por los e- liberados por NADPH+ + H+, transformándose finalmente, en 12 moléculas de gliceraldehído 3-fosfato de 3C (G3P). 4°: Estas 12 moléculas pasan por un ciclo de reordenamiento de compuestos de C, y solo 2 de ellas (c/u con 3C), formarán una molécula de 6C (hexosa), que se sintetizará en glucosa ó almidón, según la demanda de energía. Las otras 10 restantes, pasan por un proceso de regeneración, donde se combinan con 6 grupos fosfatos provenientes de 6 moléculas de ATP (y quedan 6 moléculas de ADP), y se vuelve a originar las 6 moléculas de Rubilosa difosfato (2-RuBP)con de 3C y 2 grupos P por cada molécula, que se utilizarán nuevamente para dar 2 vueltas al ciclo (1 moléc. por c/vuelta). POR LO TANTO, AL DAR 2 VUELTAS AL CICLO... 6 CO2 + 18 ATP + 12 NADPH+ + H 18 ADP + 18 P + 12 NADPH+ + C6H12O6 10.3.- Fosforilación fotosintética. Consiste en explicar cómo se obtiene la energía necesaria para sintetizar ATP a partir de las moléculas iniciales de ADP + P que se tienen al iniciar la etapa fotoquímica. El pasaje de electrones que ocurre en la etapa clara, se da SIEMPRE a favor de un gradiente de potenciales oxido-reducción, de manera que, mientras fluyen, éstos liberarán energía aprovechada para sintetizar ATP a partir de ADP y Pi. Ésta relación se explica mediante el modelo quimiosmótico de Mitchell. El mismo, propone que los e- fluyendo desde un medio negativo a otro más positivo, liberan energía que se utiliza para bombear átomos H+, a través de una membrana impermeable a ellos. La consecuencia será una diferencia de pH (espacio tilacoidal pH 4, estroma pH 8) y de potencial eléctrico entre ambos lados de esta membrana. Los H+ acumulados de un lado sólo podrán pasar mediante canales proteicos, que además tienen actividad enzimática, como ATP sintetasa. Así, el flujo de e- a través del canal genera la energía química para sintetizar ATP a partir de ADP y Pi (en el estroma). 10.4.- Importancia biológica de la fotosíntesis. La fotosíntesis es el único proceso por el cual se pueden sintetizar compuestos orgánicos, a partir de materia inorgánica. Asimismo, es el único que produce oxígeno como desecho, el cual es un sustrato esencial para la respiración celular aeróbica. Ambas transformaciones, promueve el constante funcionamiento, crecimiento y reproducción de todos los seres vivos, ya que este proceso funciona como fuente única de alimento y energía para los organismos autótrofos (primeros eslabones de las redes tróficas). A partir de ellos, tanto el alimento como la energía son transferibles al resto de los eslabones de la red. Para tener cierta dimensión de la importancia de la fotosíntesis, podemos decir que ésta radica en que, si hubiese ausencia de ella, un organismo autótrofo no podría alimentarse, ni crecer, y mucho menos reproducirse; entonces moriría, y esto desencadenaría inevitablemente la ruptura total de toda la red trófica restante.