|
Física e Introducción a la Biofísica 1P2C2019 23/10/19
TEMA 12
|
APELLIDO: |
SOBRE Nº: |
|
NOMBRES: |
Duración del examen: 1.30hs |
|
|
DNI/CI/LC/LE/PAS. Nº: |
CALIFICACIÓN: Apellido del evaluador: |
Lea atentamente cada pregunta y responda en los espacios pautados. Para las preguntas de opción múltiple marque con una X la opción correspondiente a la respuesta correcta. En todos los casos, marque una y sólo una opción . Si marca más de una opción, la pregunta será anulada.
Ejercicio N°1 (1 punto)
Unas llaves son lanzadas hacia arriba con una velocidad de 15 km/h. Calcule a qué distancia, desde su punto de partida, se encuentra las mismas cuando alcanza una velocidad de 0,34 m/s. Exprese el resultado en m
Datos: g = 9,8 m/s2
Tiro Vertical
Yo= 0m ; Vo= 15Km/h = 15000m/3600s = 4,166m/s ; Vf=0,34m/s ; g= -9,8m/s 2 (por sistema de referencia)
Vf = Vo + g . t
0,34m/s = 4,166m/s + (-9,8m/s2 ) . t
t= 0,39s
Yf = Yo + Vo . t + ½ g . t2
Yf = 0m + 4,166m/s . 0,39s + ½ . (-9,8m/s2). (0,39s) 2
Yf= 0,879m
Respuesta: ……….0,879m
Ejercicio N°2 (1 punto)
Datos: δ agua = 1 g/cm3 ; Ce agua = 1 cal/g °C; Peso de cada pesa = 9,71 N; 1 cal = 4,18 J; g = 9,8 m/s2
Q = m . Ce . (Tf – Ti); 567cm3 . 1 g/cm3 = 567g
Q = 567g . 1cal/g °C . 0,92°C
Q= 521,64 cal
2cal = 8,31J ; 521,64 cal . 8,31J / 2 cal = 2180,45 Joule (J = N.m)
W = 2 . n . P . h
2180,45 J = 2. n . 9,71N .
1,8m
n= 62,37 > se deben dejar caer 63 veces.
Respuesta: ……63 veces.
Ejercicio N°3 (1 punto)
Marque con una cruz la opción que c omplete la siguiente oración:
Cuando un cuerpo se desplaza de un punto a otro con un MRU………..
|
a) Su energía cinética es directamente proporcional a la velocidad del mismo y no depende de su masa |
|
|
|
b) Su energía cinética sólo puede ser determinada en caso de conocer su velocidad y su masa. Se puede medir en watt |
|
X |
c) Su energía cinética tiene relación directa con su masa y se mantiene constante a lo largo del trayecto descripto por el cuerpo |
|
|
d) Su energía cinética es directamente proporcional a la altura respecto de un plano de referencia y se puede medir en joule |
Ec= ½ m . v2 ; siendo la velocidad constante en MRU
Ejercicio N°4 (1 punto)
Dado un recipiente adiabático que contiene una masa inicial de hielo a -10° C, se introduce un cuerpo de 590 g en estado sólido (Ce = 0,28 cal/g °C) y pasa de una temperatura de 453 K a una temperatura final de 303 K. Calcule la masa inicial de hielo. Datos: Ce hielo = 0,5 cal/g °C; Ce agua = 1 cal/g °C; C fusión hielo = 80 cal/g;
Qa + Qc = 0 ; Qa= Qsensible hielo + Qfusion + Qsensible agua ; 453°K = 180°C ; 303°K = 30°C ; (Tf – Ti) cuerpo= -150°C
m hielo . Cehielo (Tf – Ti) + m hielo . Cfusiónhielo + magua/hielo . Ceagua (Tf – Ti)agua + mcuerpo . Ce cuerpo (Tf – Ti)cuerpo = 0
m hielo . 0,5cal/g °c . 10°C + mhielo . 80cal/g + magua/hielo . 1 cal/g °c . 30°C + 590g . 0,28 cal/g °C . -150°C = 0
m hielo . 5cal/g + mhielo . 80cal/g + m agua/hielo . 30 cal/g + (-24780 cal) = 0
m hielo . 115cal/g = 24780cal
m hielo = 215,478g
Respuesta: ………215,478g
Ejercicio N°5 (1 punto)
Determine el número de moles de oxígeno en una mezcla de gases que se encuentra en un recipiente adiabático de 0,3 m de alto, 700 mm de ancho y 52 cm de profundidad. La mezcla ejerce una presión de 590 mmHg siendo el 17 % de la misma ocupada por oxígeno y su temperatura es de -3°C.
Datos: R= 0,082 l.atm/K.mol; 760 mmHg = 1 atm = 1,013x106 barias = 1,013x105 pascales
30cm alto . 70cm ancho . 52cm profundidad =109200cm3 = 109,2L ; P.V=n.R.T ; -3°C = 270°K
760mmHg_____1atm
590mmHg____ 0,776atm
0,776atm . 109,2L = ntotales . 0,082L.atm/K.mol . 270°K
ntotales = 3,827moles
noxigeno = 3,827moles . 0,17
noxigeno = 0,65moles
Respuesta:………… 0,65moles
Ejercicio N°6 (1 punto)
En una habitación se mide la humedad relativa en 3 días diferentes del año, denominados A, B y C. En el día A la temperatura ambiente fue de 2°C, en el día B fue de 303 K y en el día C fue de -5 °C. Indique qué día presentó la mayor humedad relativa.
TA= 2°C ; TB=303°K = 30°C ; TC= -5°C
Rta: C, a menor T,menor Pv y mayor HR
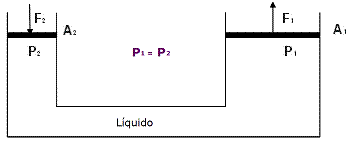
Ejercicio N°7 (1 punto)
Dato: A2 = 1/2 A1
|
X |
a) F2 < F1 |
|
b) F2 = F1 |
|
|
c) F2.A2 = F1.A 1 |
|
|
d) F2 > F1 |
F1 / A1 = F2 / A2 , siendo A2 < A1 , F2 < F1
Ejercicio N°8 (1 punto) Marque con una X la opción correcta
|
a) La conducción se produce entre dos líquidos a diferente temperatura. |
|
|
b) La radiación se puede dar en el vacío y el calor transmitido puede determinarse mediante la ley de Fourier. |
|
|
X |
c) La convección puede darse tanto en líquidos como en gases y no se corresponde con la ley de Fourier. |
|
d) La conducción se puede producir entre dos extremos de un sólido que se encuentran a la misma temperatura. |
Ejercicio N°9 (1 punto)
Calcule cual es la máxima masa de vapor que puede contener una pecera de 60 cm de largo, 20 cm de ancho y 30 cm de alto, si se comienza a llenar de vapor y alcanza una humedad relativa del 30% cuando su humedad absoluta es de 2500 g/m3
dimensiones: 0,6m . 0,2m . 0,3m=0,036m3 ; HR= H absoluta/H máxima
0,30= 2500 g/m3 / H máxima
8333,333g/m3 = H máxima
1m3________8333,333g
0,036m3_____ 300g
Respuesta:…………. 300g
Ejercicio N°10 (1 punto)
Determine la variación de energía interna (en calorías) de un proceso donde 88 g de un gas ideal se expanden a una presión constante de 0,8 atm siendo la variación de volumen de 5 L y la variación de temperatura de 15 K,
Datos: Cep = 0,24 cal/g °C; R = 0,082 l atm/mol K = 2 cal/mol K = 8,31 J/mol K
W=P.(Vf-Vi) ; ΔT=20°C ; ΔU=Q-W
W= 0,8atm . 5 L = 4L.atm
Q= m . Ce . Δ T
Q= 88g . 0,24 cal/g °C . 15°C
2cal = 0,082 L.atm ; Q= 316,8 cal . 0,082 L.atm / 2cal = 12,988 L.atm
Δ U= 12,988 L.atm - 4L.atm
ΔU= 8,988 L.atm = 219,219 cal
Respuesta: …………..219,219 cal
